짚신벌레
원생생물 · 아메바조아
Paramecium caudatum
학명 유래: "속명 Paramecium은 그리스어 paramēkēs(길쭉한, oblong)에서 유래하였으며, 종소명 caudatum은 라틴어로 '꼬리가 있는(tailed)'이라는 의미로 세포 후단부가 뾰족하게 테이퍼진 형태학적 특징을 반영한다"
발견
미생물 특성
분류
서식지
분류 변천사
1674년경 Leeuwenhoek이 Paramecium 속 최초 관찰 추정, 1752년 John Hill이 Paramecium이라는 용어 최초 사용, 1773년 Otto Friedrich Müller가 속명을 린네식 분류 체계에 공식 도입, 1833년 Christian Gottfried Ehrenberg가 P. caudatum 종을 최초 기재. 현대 분자계통학에서 SAR 상위군 > Alveolata > Ciliophora > Oligohymenophorea > Peniculida > Parameciidae에 배치(NCBI Taxon ID 5885)
임상적 의미
비병원성 자유 생활 원생생물로 인체 감염과 무관. 생태독성학 지표생물 및 생물학 연구 모델 생물로서 과학적 가치가 큼

짚신벌레(Paramecium caudatum Ehrenberg, 1833)는 섬모충문(Ciliophora) 올리고히메노포레아강(Oligohymenophorea) 페니쿨리다목(Peniculida) 짚신벌레과(Parameciidae)에 속하는 단세포 진핵생물이다. 전 세계 담수, 기수 및 해수 환경에서 광범위하게 분포하는 자유 생활 원생생물로, 비병원성이며 인체에 감염을 일으키지 않는다. 세포 길이는 170~330 μm(일반적으로 200~300 μm)에 달하며, 세포 전체 표면을 덮고 있는 약 4,000개의 운동성 섬모(motile cilia)가 협응적 박동(metachronal wave)을 통해 나선형 경로로 유영하는 것이 특징이다(Bouhouche et al., 2022). 종소명 "caudatum"은 라틴어로 "꼬리가 있는(tailed)"이라는 의미로, 세포 후단부가 뾰족하게 테이퍼진 형태에서 유래하였으며, 초기 현미경학자들은 이 생물의 전체 형태를 슬리퍼에 비유하여 "슬리퍼 동물(slipper animalcule)"이라는 별칭으로 불렀다.
P. caudatum은 섬모충류 연구의 대표적 모델 생물로서, "섬모충류의 흰쥐(white rat of the Ciliophora)"라는 별명을 가지고 있다(Van Houten, 2023). 1934년 러시아 생태학자 게오르기 가우제(Georgy Gause)는 P. caudatum과 P. aurelia를 이용한 경쟁 실험으로 현대 생태학의 기본 원리인 경쟁적 배타 원리(competitive exclusion principle)를 정립하였다(Gause, 1934). 또한 이 종은 핵 이형성(nuclear dimorphism), 프로그래밍된 게놈 재배열, 섬모 운동의 이온 채널 메커니즘 연구에서 핵심적인 역할을 해왔으며, 단세포이면서도 칼슘 기반 활동 전위에 의해 복잡한 회피 반응을 보여 "유영하는 뉴런(swimming neuron)"이라는 독특한 명칭으로도 불린다(Brette, 2021).
생물안전 측면에서 P. caudatum은 BSL-1 수준의 비병원성 생물로, 특별한 취급 제한 없이 연구 및 교육 목적으로 널리 배양된다. IUCN 적색목록에 등재되어 있지 않으며, 전 세계적으로 개체수가 풍부하여 현재 보전 위협 상태에 있지 않다.
1. 개요
짚신벌레의 속명 Paramecium은 그리스어 "paramēkēs"(길쭉한, oblong)에서 유래하였고, 종소명 "caudatum"은 라틴어로 "꼬리가 있는(tailed)"이라는 뜻으로 세포 후단부의 뾰족한 형태를 반영한다. 한국어 일반명 "짚신벌레"는 세포의 전체 윤곽이 짚신(짚으로 만든 전통 신발)을 닮은 데서 유래하였으며, 영어권에서는 "slipper animalcule"이라는 별칭이 사용된다.
P. caudatum은 현재 NCBI Taxonomy에서 Taxon ID 5885로 등록되어 있으며, SAR 상위군(supergroup) 내 피막류(Alveolata)의 섬모충문(Ciliophora)에 분류된다. 동일 속 내에는 15개 이상의 형태종(morphospecies)이 인정되고 있다(Fokin, 2010). 이 종은 가장 두드러진 특징으로 핵 이형성을 가지는데, 체세포 기능을 담당하는 다배체 대핵(macronucleus)과 생식계열 유전정보를 보존하는 2배체 소핵(micronucleus) 1개를 보유한다.
2. 분류와 계통
P. caudatum의 현대적 분류 체계는 분자계통학적 증거를 기반으로 구축되었으며, SAR 상위군(Stramenopila-Alveolata-Rhizaria) 내 피막류(Alveolata)에 배치된다. 피막류 내에서 섬모충류(Ciliophora)는 와편모충류(Dinoflagellata), 정단복합체충류(Apicomplexa)와 자매군 관계를 형성한다. 상세 분류 체계는 다음과 같다: 역(Domain) Eukaryota, 분기군(Clade) SAR, 상문(Superphylum) Alveolata, 문(Phylum) Ciliophora, 강(Class) Oligohymenophorea, 목(Order) Peniculida, 과(Family) Parameciidae, 속(Genus) Paramecium Müller, 1773, 종(Species) P. caudatum Ehrenberg, 1833.
Paramecium 속의 계통학적 연구는 주로 18S rRNA 유전자, ITS 영역, 미토콘드리아 COI 유전자 등을 이용한 분자계통분석에 기반한다. Strüder-Kypke et al.(2000)의 18S rRNA 기반 계통분석은 Paramecium 종들이 최소 4개의 분기군(clade)을 형성하며, P. aurelia 아군이 가장 파생적인 위치에 있음을 보여주었다. P. caudatum은 P. aurelia 종 복합체의 자매군에 해당하며, 두 계통은 가장 오래된 1회의 전체 게놈 중복(WGD)만을 공유한다(McGrath et al., 2014).
속명 Paramecium은 1773년 덴마크의 동물학자 오토 프리드리히 뮬러(Otto Friedrich Müller)가 린네식 분류 체계에 공식적으로 도입하였으나, 이 용어 자체는 1752년 런던의 존 힐(John Hill) 박사가 처음 사용한 것으로 기록되어 있다. P. caudatum 종은 1833년 독일의 자연주의자 크리스티안 고트프리트 에렌베르크(Christian Gottfried Ehrenberg)에 의해 최초 기재되었다(Fokin, 2010). Paramecium 속의 최초 관찰은 1674년경 네덜란드의 현미경학 선구자 안토니 반 레이우엔훅(Antonie van Leeuwenhoek)에 의해 이루어진 것으로 추정되며, 1678년 크리스티안 하위헌스(Christiaan Huygens)가 왕립학회(Royal Society)에 보낸 서신에서 명확히 기술되어 있다.
Paramecium 속 내에서 P. caudatum은 비교적 대형 종에 속하며, 1개의 소핵을 가지는 점에서 2개의 소핵을 가진 P. aurelia 종 복합체와 구별된다. 동일 속 내 주요 형태종으로는 P. aurelia(15개 잠재종으로 구성된 종 복합체), P. bursaria(녹색 공생 조류 보유), P. multimicronucleatum(3~7개 소핵 보유), P. tetraurelia(게놈 연구 모델) 등이 있다.
3. 형태와 구조
P. caudatum은 방추형(spindle-shaped)의 단세포로, 전단부는 둥글고 후단부는 뾰족하게 테이퍼진다. 세포 길이는 170~330 μm이며, 일반적으로 200~300 μm 범위로 Paramecium 속 중 비교적 대형에 해당한다(Fokin, 2010). 세포 폭은 약 45~80 μm이다(Wichterman, 2012). 크기가 비교적 크기 때문에 육안으로도 희미하게 흰 점처럼 관찰할 수 있으며, 일반 광학현미경 저배율에서 쉽게 확인된다.
세포 표면은 표피(pellicle)로 덮여 있으며, 표피는 세포막과 그 바로 아래의 피막소포(alveolar sacs)로 구성된다. 표피 아래에는 방추형의 방출체인 트리코시스트(trichocyst)가 조밀하게 분포하여, 위협 시 폭발적으로 방출되어 방어 기능을 수행한다(Harumoto & Miyake, 1991). 세포의 복측 전반부에는 구강구(oral groove, vestibulum)가 위치하며, 이는 세포 깊숙이 함입된 구강(buccal cavity)으로 연결된다. 구강 끝에는 세포구(cytostome)가 있고, 이어서 세포인두(cytopharynx)가 위치하여 먹이 입자를 세포 내로 유도한다.
세포 전체 표면은 약 4,000개의 운동성 섬모로 균일하게 덮여 있으며, 이들은 종방향 열(longitudinal rows)로 배열되어 있다(Bouhouche et al., 2022). 개별 섬모의 길이는 10~12 μm, 직경은 약 0.27 μm이며, 9+2 미세소관 구조의 축사(axoneme)를 가진다. 후단부에는 길이 10~20 μm의 미모속(caudal cilia)이 존재하며, 특징적으로 외측으로 굽어 있다. P. caudatum은 전단부와 후단부에 각각 하나씩, 총 2개의 수축포(contractile vacuole)를 가지며(Patterson, 1980), 각 수축포는 방사상으로 배열된 집합관(collecting canal)과 연결되어 특징적인 별 모양을 형성한다. 수축포는 저장성 담수 환경에서 세포 내로 유입되는 과잉 수분을 배출하여 삼투압을 조절한다.
P. caudatum의 가장 독특한 구조적 특징은 핵 이형성(nuclear dimorphism)이다(Mikami, 1988). 대핵(macronucleus)은 큰 강낭콩 모양의 다배체 핵으로 세포 대사, 영양, 호흡 등 일상적 체세포 기능을 조절하며 전사 활성이 매우 높다. 소핵(micronucleus)은 작고 조밀한 2배체 핵으로 유성생식(접합) 시 감수분열과 유사분열을 수행하여 생식계열 유전정보를 보존한다. P. caudatum은 1개의 소핵만을 가지는데, 이는 2개의 소핵을 가진 P. aurelia와 구별되는 주요 형태학적 특징이다.
4. 유전체와 분자생물학
P. caudatum은 모든 섬모충류와 마찬가지로 두 가지 유형의 핵 유전체를 보유한다. 생식계열 유전체(소핵 게놈)는 약 1,300~5,500 Mb로 추정되며, 이는 섬모충류 중 가장 큰 생식계열 게놈 규모에 해당한다(McGrath et al., 2014; Furrer et al., 2024). 체세포 유전체(대핵 게놈)는 프로그래밍된 DNA 제거(programmed DNA elimination)를 통해 생식계열 유전체의 약 2%만이 유지되는데, 이는 생물계에서 가장 극단적인 게놈 재배열 사례 중 하나이다.
2014년 McGrath et al.에 의해 발표된 P. caudatum 대핵 게놈 시퀀싱 결과에 따르면, 대핵 게놈 조립체(assembly)는 약 30.5 Mb로, P. aurelia 종 복합체의 대핵 게놈(68~77 Mb)의 절반 이하이다. 이 게놈에는 18,509개의 단백질 코딩 유전자가 주석(annotation)되어 있으며, 이는 P. aurelia 종들의 유전자 수(약 34,000~40,000개)의 약 절반에 해당한다. 대핵 게놈의 GC 함량은 28.2%로 AT가 풍부하며, 평균 인터진(intergenic) 영역 길이가 110 bp에 불과하여 진핵생물 중 가장 컴팩트한 게놈 구조 중 하나를 보인다(McGrath et al., 2014).
계통학적 분석을 통해 P. caudatum은 P. aurelia 종 복합체가 경험한 세 차례의 전체 게놈 중복(whole-genome duplication, WGD) 중 가장 오래된 한 차례(약 15억 년 전으로 추정)만을 공유하는 것으로 확인되었다. 나머지 두 차례의 WGD(중간 및 최근)는 P. aurelia 계통에서만 발생하였다. 흥미롭게도 P. caudatum은 고대 WGD 유래 중복 유전자의 약 16%를 여전히 유지하고 있는데, 이는 P. aurelia 종들의 유지율(약 8%)의 두 배에 해당하며, 후속 WGD가 고대 중복 유전자에 대한 유전자 용량(dosage) 제약을 완화시킨다는 가설을 지지한다(McGrath et al., 2014). 2025년 발표된 최신 연구에서는 Paramecium 속 5종의 대핵 게놈 분석을 통해 종간 게놈 크기가 47.78~113.16 Mb 범위로 예상 외의 다양성을 보인다고 보고하였다(Li et al., 2025).
미토콘드리아 게놈은 선형 구조를 가지며, 2011년 Barth & Behnke에 의해 완전 시퀀싱되었다. P. caudatum의 미토콘드리아 게놈은 P. tetraurelia와 비교하여 뉴클레오타이드 조성 및 코돈 사용 양식에서 유의한 차이를 보이며, 이는 속 내에서도 미토콘드리아 진화가 활발하게 진행되고 있음을 시사한다.
5. 생태와 환경적 역할
P. caudatum은 전 세계적 분포(cosmopolitan distribution)를 보이는 종으로, 남극을 제외한 모든 대륙에서 분리된 기록이 있다(Fokin, 2010). 주요 서식 환경은 담수 서식지로서 연못, 호수, 하천, 저수지, 농업용 수로 등이며, 특히 부패하는 유기물이 풍부한 정체 수역에서 높은 밀도로 발견된다. 기수 및 해양 환경에서도 발견되나 담수 환경에 비해 출현 빈도가 낮다. 연안 담수 환경(littoral freshwater environments)의 진흙-물 경계면(mud-water interface)에 풍부하게 서식한다.
P. caudatum은 종속영양생물(heterotroph)로서 세균, 효모, 단세포 조류 및 미세 유기물 입자를 섭식한다. 구강구의 섬모가 협응적으로 박동하여 주변의 먹이 입자를 물과 함께 끌어들이고, 세포구를 통해 식포(food vacuole)가 형성된다. 식포는 세포질 내에서 회전 운동(cyclosis)을 하며 리소좀과 융합하여 소화가 진행되고, 소화되지 않은 잔여물은 세포항문(cytoproct)을 통해 배출된다. 이러한 세균 섭식 활동은 담수 생태계의 미생물 먹이그물(microbial food web)에서 중요한 역할을 하며, 세균 군집 구조 조절과 영양소 재순환에 기여한다.
생태학적으로 P. caudatum은 환경 조건에 대한 높은 적응력을 보인다. 최적 생장 온도는 약 24~29°C이며(Krenek et al., 2012), 7~35.5°C 범위에서 성장이 가능하다. 최적 pH는 6.0~7.0 범위이며, 저산소 조건에서는 pH 4.7~6.7이 생존에 적합한 것으로 보고되어 있다(Heydarnejad, 2008). 호기성 생물로서 산소가 풍부한 환경을 선호하지만, 단기적으로 저산소 조건에서도 생존할 수 있다. 담수 환경에서는 수축포를 통해 삼투압을 효과적으로 조절하며, 온도 및 화학적 자극에 대해 주화성(chemotaxis)과 주열성(thermotaxis) 반응을 통해 적응한다.
P. caudatum의 주요 천적은 육식성 섬모충인 Didinium nasutum이다. Didinium-Paramecium 시스템은 포식자-피식자 상호작용 연구의 고전적 모델로, 로트카-볼테라(Lotka-Volterra) 개체군 동태 모델의 실험적 검증에 광범위하게 활용되어 왔다. P. caudatum은 포식자에 대응하여 트리코시스트를 폭발적으로 방출하는 방어 메커니즘을 가지며, 이를 통해 포식자의 공격 범위를 벗어나거나 독소를 중화할 수 있다(Harumoto & Miyake, 1991; Miyake, 1996).
P. caudatum은 여러 종의 세포내 공생 세균(intracellular endosymbiont)의 숙주로 알려져 있다. 대표적인 공생체는 Holospora 속의 알파프로테오박테리아로, H. obtusa는 대핵 특이적, H. undulata와 H. recta는 소핵 특이적 공생체이다(Görtz et al., 2009). 이들 공생체는 숙주의 식포를 통해 세포 내로 유입된 후 특정 핵으로 이동하여 감염을 확립한다. 주목할 만한 것은 Holospora 감염이 숙주에게 열 스트레스 및 산화 스트레스에 대한 저항성을 부여하는 것으로 보고된 점이다(Hori & Fujishima, 2003).
6. 연구사와 과학적 의의
Paramecium 속의 최초 관찰은 1674년경 안토니 반 레이우엔훅에 의해 이루어진 것으로 추정되며, 1678년 크리스티안 하위헌스가 왕립학회에 보낸 서신에서 이 생물에 대한 기술이 명확히 남아 있다. 1752년 존 힐이 "Paramecium"이라는 용어를 처음 사용하였고, 1773년 뮬러가 이를 린네식 분류 체계에 공식 도입하였다. P. caudatum 종은 1833년 에렌베르크에 의해 최초로 기재되었으며, 이후 100년 이상에 걸쳐 세포생물학, 유전학, 생태학의 핵심 연구 모델로 자리 잡았다.
가장 대표적인 연구 이정표는 1934년 게오르기 가우제의 경쟁적 배타 원리(competitive exclusion principle, Gause's law) 정립이다(Gause, 1934). 가우제는 P. caudatum과 P. aurelia를 동일 배지에서 함께 배양했을 때, 동일한 자원을 더 효율적으로 이용하는 P. aurelia가 P. caudatum을 경쟁적으로 배제하는 현상을 관찰하였다. 이 실험은 "두 종이 동일한 생태적 지위를 무한정 공유할 수 없다"는 생태학의 기본 원리를 확립한 기념비적 연구로 평가받는다.
P. caudatum은 모델 생물로서 다양한 분야에서 활용된다. 세포생물학 및 유전학 분야에서는 핵 이형성, 프로그래밍된 게놈 재배열, 비멘델 유전 현상 연구에 활용된다. 섬모 생물학 분야에서는 약 4,000개의 운동성 섬모를 가진 이 종이 인간 섬모병증(ciliopathies) 연구의 모델로서 섬모 박동 메커니즘과 기저체 구조 연구에 기여하고 있다(Valentine & Van Houten, 2021). 신경생리학 분야에서는 칼슘 기반 활동 전위에 의해 촉발되는 회피 반응(avoiding reaction)이 다세포 생물의 신경세포 신호 전달과 유사하여, 이온 채널에 의한 행동 조절 메커니즘 연구의 단세포 모델로 활용된다(Brette, 2021). 또한 생태독성학에서는 환경 오염 물질의 독성 평가를 위한 생물검정(bioassay) 대상으로, 교육 현장에서는 현미경 관찰 실습과 세포생물학 교육의 표준 교재 생물로 널리 활용된다.
2014년 P. caudatum 대핵 게놈의 완전 시퀀싱(McGrath et al., 2014)은 Paramecium 속 게놈 진화 연구에 새로운 전기를 마련하였으며, 2024년에는 RNA 간섭(RNAi) 및 단백질 국소화 기술이 P. caudatum에 적용되어 이 종의 분자 도구 활용 범위가 크게 확대되었다(Furrer et al., 2024).
7. 번식과 생활사
P. caudatum의 주된 번식 방식은 횡분열(transverse binary fission)이다. 최적 조건(24~28°C)에서 하루에 2~3회 분열할 수 있으며, 한 번의 분열 주기에는 약 6~8시간이 소요된다(Wichterman, 2012). 이분법 과정에서 대핵은 비유사분열(amitosis)로, 소핵은 유사분열(mitosis)로 분열한 후 세포가 횡방향으로 나뉘어 각 딸세포가 대핵과 소핵을 하나씩 받게 된다.
접합(conjugation)은 P. caudatum의 유성생식 과정으로, 유전적 다양성을 창출하고 클론 노화를 방지하는 핵심 기능을 한다. 양립 가능한 교배형(mating type)을 가진 두 개체가 일시적으로 융합하여 유전 물질을 교환하며, 이 과정에서 각 개체의 소핵이 감수분열을 수행하여 반수체 배우자핵을 형성하고, 이것이 상대 개체로 이동하여 융합한 후 새로운 대핵과 소핵이 분화된다. P. caudatum에서는 자가수정의 한 형태인 세포교합(cytogamy)도 유도할 수 있다(Yanagi & Haga, 1998).
P. caudatum 클론의 미성숙기(immaturity period)는 약 60회 분열이며, 접합이나 자가수정 없이 무성생식만 지속할 경우 약 600회 분열 후 클론 사멸(clonal death)에 이른다(Uezu et al., 2009). 개별 계통의 총 수명은 250~750회 분열 범위로 다양하게 보고되어 있으며(Komori et al., 1979), 접합이나 자가수정을 통한 핵 재편성은 세포 회춘(rejuvenation) 효과를 가져 클론 수명을 연장한다. 이러한 클론 노화-회춘 시스템은 유성생식의 진화적 이점을 연구하는 데 중요한 모델을 제공한다.
8. 근연종 비교
| 종명 | 세포 길이 (μm) | 소핵 수 | 형태적 특징 | WGD 횟수 | 특이 사항 |
|---|---|---|---|---|---|
| P. caudatum | 170~330 | 1 | 방추형, 후단 뾰족 | 1회 | 가우제 실험 대상, 게놈 ~30.5 Mb |
| P. aurelia (복합종) | 80~170 | 2 | 타원형, 후단 둥근 | 3회 | 15개 잠재종, 게놈 68~77 Mb |
| P. bursaria | 80~150 | 1 | 난형, 넓은 구강구 | - | Chlorella 공생, 녹색 |
| P. multimicronucleatum | 200~350 | 3~7 | 방추형, 대형 | - | 다수 소핵 보유 |
| P. tetraurelia | 100~150 | 2 | 방추형 | 3회 | 게놈 연구 표준 모델 |
가우제의 경쟁적 배타 실험에서 P. aurelia가 P. caudatum을 경쟁적으로 배제한 것은 동일 자원에 대한 이용 효율의 차이에 기인한다. 반면 P. bursaria는 세포 내 공생 조류 Chlorella를 통한 광합성으로 추가적인 탄소원을 확보할 수 있어, 다른 Paramecium 종과 니치를 달리하여 공존이 가능하다. 게놈 규모 측면에서 P. caudatum의 대핵 게놈(약 30.5 Mb)은 P. aurelia 종들(68~77 Mb)의 절반 이하로, 이는 P. aurelia 계통에서만 발생한 두 차례의 추가 WGD에 기인한다(McGrath et al., 2014).
재미있는 사실
짚신벌레는 단세포 생물이지만 약 4,000개의 섬모를 협응적으로 박동시켜 나선형으로 유영할 수 있으며, 이 복잡한 운동 제어 능력 때문에 일부 과학자들은 짚신벌레를 '유영하는 뉴런(swimming neuron)'이라고 부른다(Brette, 2021).
짚신벌레의 회피 반응은 칼슘 기반 활동 전위에 의해 촉발되며, 이는 인간 신경세포의 신호 전달 메커니즘과 놀라울 정도로 유사하다. 뇌도 없는 단세포 생물이 뉴런과 같은 전기 신호를 사용하는 것이다.
1934년 러시아 생태학자 게오르기 가우제는 짚신벌레를 이용한 실험으로 현대 생태학의 기본 원리인 '경쟁적 배타 원리(가우제의 법칙)'를 정립하였다. 이 원리는 동일한 생태적 지위를 차지하는 두 종이 무한정 공존할 수 없다는 것이다(Gause, 1934).
짚신벌레의 생식계열 게놈(소핵)은 최대 5,500 Mb에 달하지만, 체세포핵(대핵)에는 그 중 약 2%(약 30.5 Mb)만이 유지된다. 나머지 98%는 프로그래밍된 DNA 제거를 통해 삭제되는데, 이는 생물계에서 가장 극단적인 게놈 재배열 사례 중 하나이다(McGrath et al., 2014).
짚신벌레의 대핵 게놈은 약 30.5 Mb에 18,509개의 유전자가 담겨 있으며, 유전자 사이의 평균 간격(인터진 영역)이 겨우 110 bp로 진핵생물 중 가장 조밀한 게놈 구조를 가진다(McGrath et al., 2014).
짚신벌레는 수축포(contractile vacuole)를 이용해 삼투압을 조절한다. 담수 환경에서 세포 내로 끊임없이 유입되는 과잉 수분을 별 모양의 수축포 2개가 수집하여 외부로 배출함으로써 세포가 터지는 것을 방지한다(Patterson, 1980).
짚신벌레는 트리코시스트(trichocyst)라는 방추형 방출체를 표피 아래에 수천 개 보유하고 있다. 위협을 받으면 밀리초 단위로 이를 폭발적으로 방출하여 포식자의 공격 범위를 벗어나거나 독소를 중화할 수 있다(Miyake, 1996).
짚신벌레의 주요 천적인 육식성 섬모충 Didinium nasutum은 자신보다 훨씬 큰 짚신벌레를 통째로 삼킬 수 있다. 이 둘의 포식자-피식자 관계는 로트카-볼테라 개체군 동태 모델을 실험적으로 검증하는 고전적 모델이다.
짚신벌레는 Holospora 속 세균과 세포내 공생 관계를 맺을 수 있는데, 이 공생 세균에 감염된 짚신벌레는 감염되지 않은 개체보다 열 스트레스와 산화 스트레스에 대한 저항성이 높아지는 것으로 보고되어 있다(Hori & Fujishima, 2003).
짚신벌레 클론은 무성생식만 계속하면 약 600회 분열 후 '클론 사멸'에 이른다. 그러나 접합(유성생식)을 통해 유전 물질을 교환하면 '회춘' 효과가 나타나 수명이 연장되는데, 이는 유성생식이 왜 진화적으로 유지되는지를 보여주는 대표적 사례이다(Uezu et al., 2009).
짚신벌레라는 한국어 이름은 세포의 전체 윤곽이 짚으로 만든 전통 신발인 '짚신'을 닮은 데서 유래하였고, 영어권에서는 '슬리퍼 동물(slipper animalcule)'이라 불린다. 서로 다른 문화에서 같은 '신발' 비유가 사용된 것이 흥미롭다.
FAQ
짚신벌레(Paramecium caudatum)의 세포 길이는 170~330 μm(마이크로미터)이며, 일반적으로 200~300 μm 범위입니다. 이는 약 0.2~0.3 mm로, 맨눈으로도 희미하게 흰 점처럼 보일 수 있는 크기입니다. Paramecium 속 중에서 비교적 큰 종에 속하며, P. aurelia(80~170 μm)보다 약 2배 정도 큽니다(Fokin, 2010).
짚신벌레는 세포 표면을 덮고 있는 약 4,000개의 섬모(cilia)가 파동 형태로 협응적 박동(metachronal wave)을 일으켜 움직입니다(Bouhouche et al., 2022). 이로 인해 나선형 경로를 따라 유영하면서 동시에 장축을 기준으로 회전합니다. 평균 유영 속도는 약 1,000~2,000 μm/s(초당 약 1~2 mm)로, 체장의 약 5~10배에 달하는 거리를 매초 이동합니다(Brette, 2021).
짚신벌레는 종속영양생물로서 주로 세균, 효모, 단세포 조류 등을 섭식합니다. 세포 복측에 위치한 구강구(oral groove)의 섬모가 박동하여 먹이 입자를 물과 함께 세포 내로 끌어들이고, 세포구(cytostome)에서 식포(food vacuole)가 형성되어 리소좀 효소에 의한 세포내 소화가 진행됩니다. 소화되지 않은 찌꺼기는 세포항문(cytoproct)을 통해 배출됩니다.
짚신벌레의 주된 번식 방식은 무성생식인 이분법(binary fission)입니다. 최적 조건에서 하루에 2~3회 분열할 수 있으며, 한 번의 분열 주기에는 약 6~8시간이 소요됩니다(Wichterman, 2012). 또한 접합(conjugation)이라는 유성생식 과정을 통해 두 개체가 유전 물질을 교환하여 유전적 다양성을 창출하고 클론 노화를 방지합니다.
짚신벌레를 포함한 모든 섬모충류는 핵 이형성(nuclear dimorphism)이라는 독특한 특징을 가집니다. 대핵(macronucleus)은 다배체 핵으로 세포 대사, 영양, 호흡 등 일상적인 체세포 기능을 조절하고, 소핵(micronucleus)은 2배체 핵으로 유성생식 시 생식계열 유전정보를 보존하고 전달합니다. 이러한 '기능 분업'은 세포가 활발한 유전자 발현과 생식 능력을 동시에 유지할 수 있게 해줍니다(Catania et al., 2024).
짚신벌레 클론의 수명은 분열 횟수로 측정됩니다. 접합이나 자가수정 없이 무성생식만 지속할 경우 약 600회 분열 후 클론 사멸(clonal death)에 이릅니다(Uezu et al., 2009). 그러나 접합을 통한 핵 재편성은 세포 회춘 효과를 가져 클론 수명을 연장하며, 개별 계통의 총 수명은 250~750회 분열 범위로 보고되어 있습니다(Komori et al., 1979).
짚신벌레는 남극을 제외한 전 세계 대륙에서 발견되는 범세계적 분포 종입니다. 특히 연못, 호수, 하천, 저수지, 농업용 수로 등 유기물이 풍부하고 세균이 번성하는 정체된 담수 환경에서 높은 밀도로 출현합니다. 기수 및 해수 환경에서도 드물게 발견됩니다(Fokin, 2010).
짚신벌레는 '회피 반응(avoiding reaction)'이라는 특징적인 방어 행동을 보입니다. 기계적·화학적·열적 자극을 받으면 칼슘 이온의 유입에 의해 섬모 박동 방향이 역전되어 후진 유영을 하고, 방향을 전환한 뒤 다시 전진합니다(Brette, 2021). 또한 표피 아래의 트리코시스트(trichocyst)를 폭발적으로 방출하여 포식자로부터 탈출하거나 독소를 중화하는 방어 메커니즘도 가지고 있습니다(Miyake, 1996).
짚신벌레는 '섬모충류의 흰쥐'로 불릴 만큼 중요한 모델 생물입니다. 1934년 가우제의 경쟁적 배타 원리 실험(Gause, 1934), 핵 이형성과 게놈 재배열 연구, 섬모 생물학 및 인간 섬모병증 연구(Valentine & Van Houten, 2021), 이온 채널에 의한 행동 조절 연구(Brette, 2021) 등 다양한 분야에서 핵심적인 역할을 합니다. 비교적 큰 크기, 용이한 배양, 활발한 운동성 덕분에 교육 현장에서도 널리 활용됩니다.
짚신벌레는 생식계열 게놈(소핵)이 약 1,300~5,500 Mb로 매우 크지만, 체세포핵(대핵)에는 그 중 약 2%(약 30.5 Mb)만이 유지됩니다. 나머지 98%는 프로그래밍된 DNA 제거를 통해 삭제되는데, 이는 생물계에서 가장 극단적인 게놈 재배열 사례 중 하나입니다. 대핵 게놈에는 18,509개의 유전자가 포함되어 있으며, 평균 인터진 영역이 110 bp에 불과하여 진핵생물 중 가장 컴팩트한 게놈 구조를 보입니다(McGrath et al., 2014).
Paramecium 속에는 15개 이상의 형태종이 인정됩니다. P. aurelia는 15개 잠재종으로 구성된 종 복합체로 더 작고(80~170 μm) 소핵 2개를 가집니다. P. bursaria는 녹색 공생 조류 Chlorella를 세포 내에 보유하여 녹색을 띱니다. P. multimicronucleatum은 P. caudatum과 비슷한 크기이지만 3~7개의 소핵을 가지며, P. tetraurelia는 게놈 연구의 표준 모델로 활용됩니다(Fokin, 2010).
📚참고문헌
Barth, D., & Behnke, A. (2011). The mitochondrial genome sequence of the ciliate Paramecium caudatum reveals a shift in nucleotide composition and codon usage within the genus Paramecium. BMC Genomics, 12, 272. https://doi.org/10.1186/1471-2164-12-272
Bouhouche, K., Yano, J., & Valentine, M. S. (2022). Paramecium, a model to study ciliary beating and ciliogenesis. Frontiers in Cell and Developmental Biology, 10, 847908. https://doi.org/10.3389/fcell.2022.847908
Brette, R. (2021). Integrative neuroscience of Paramecium, a "swimming neuron". eNeuro, 8(3), ENEURO.0018-21.2021. https://doi.org/10.1523/ENEURO.0018-21.2021
Catania, F., Vitali, V., Rothering, R., & Zufall, R. A. (2024). Paramecium genetics, genomics, and evolution. Annual Review of Genetics, 58, 1-25. https://doi.org/10.1146/annurev-genet-071819-104035
Fokin, S. I. (2010). Paramecium genus: biodiversity, some morphological features and the key to the main morphospecies discrimination. Protistology, 6(4), 227-235. https://www.zin.ru/journals/protistology/num6_4/fokin_227-235.pdf
Furrer, H., et al. (2024). Application of RNA interference and protein localization to study Paramecium caudatum. Communications Biology, 7, 246. https://doi.org/10.1038/s42003-024-05906-2
Gause, G. F. (1934). The Struggle for Existence. Williams and Wilkins.
Görtz, H. D., Strüder-Kypke, M., & Zeini, A. (2009). Holospora and Caedibacter: Endosymbionts of Paramecium. In Endosymbionts in Paramecium (pp. 161-176). Springer.
Harumoto, T., & Miyake, A. (1991). Defensive function of trichocysts in Paramecium. Journal of Experimental Zoology, 260(1), 84-92. https://doi.org/10.1002/jez.1402600111
Heydarnejad, M. S. (2008). Survival of Paramecium caudatum at various pH values and under hypoxic condition. Pakistan Journal of Biological Sciences, 11(3), 392-397. https://doi.org/10.3923/pjbs.2008.392.397
Hori, M., & Fujishima, M. (2003). The endosymbiotic bacterium Holospora obtusa enhances heat-shock gene expression of the host Paramecium caudatum. Journal of Eukaryotic Microbiology, 50(4), 293-298. https://doi.org/10.1111/j.1550-7408.2003.tb00137.x
Komori, R., Sato, H., Harumoto, T., & Takagi, Y. (1979). Clonal death associated with the number of fissions in Paramecium caudatum. Journal of Cell Science, 41(1), 177-191. https://doi.org/10.1242/jcs.41.1.177
Krenek, S., Petzoldt, T., &128, T. (2012). Thermal performance curves of Paramecium caudatum: A model selection approach. European Journal of Protistology, 48(2), 124-130. https://doi.org/10.1016/j.ejop.2011.07.004
Lynn, D. H. (2010). The Ciliated Protozoa: Characterization, Classification, and Guide to the Literature (3rd ed.). Springer. https://doi.org/10.1007/978-1-4020-8239-9
McGrath, C. L., Gout, J. F., Doak, T. G., Yanagi, A., & Lynch, M. (2014). Insights into three whole-genome duplications gleaned from the Paramecium caudatum genome sequence. Genetics, 197(4), 1417-1428. https://doi.org/10.1534/genetics.114.163287
Mikami, K. (1988). Nuclear differentiation in Paramecium caudatum. Zoological Science, 5, 915-926.
Miyake, A. (1996). Defensive function of trichocysts in Paramecium against the predatory ciliate Monodinium balbiani. European Journal of Protistology, 32, 128-133. https://doi.org/10.1016/S0932-4739(96)80048-4
Patterson, D. J. (1980). Contractile vacuoles and associated structures: their organization and function. Biological Reviews, 55(1), 1-46. https://doi.org/10.1111/j.1469-185X.1980.tb00686.x
Strüder-Kypke, M. C., Wright, A.-D. G., Fokin, S. I., & Lynn, D. H. (2000). Phylogenetic relationships of the Subclass Peniculia (Oligohymenophorea, Ciliophora) inferred from small subunit rRNA gene sequences. Journal of Eukaryotic Microbiology, 47(3), 419-429. https://doi.org/10.1111/j.1550-7408.2000.tb00069.x
Uezu, T., Takei, Y., & Hiwatashi, K. (2009). Novel features of computer-simulated clonal life of Paramecium caudatum. Journal of Theoretical Biology, 259(1), 143-150. https://doi.org/10.1016/j.jtbi.2009.01.034
Valentine, M. S., & Van Houten, J. L. (2021). Using Paramecium as a model for ciliopathies. Genes, 12(10), 1493. https://doi.org/10.3390/genes12101493
Van Houten, J. L. (2023). A review for the special issue on Paramecium as a modern model organism. Microorganisms, 11(4), 890. https://doi.org/10.3390/microorganisms11040890
Wichterman, R. (2012). The Biology of Paramecium (2nd ed.). Springer. ISBN 978-1-4757-0372-6.
Yanagi, A., & Haga, N. (1998). Induction of conjugation by methyl cellulose in Paramecium caudatum. Zoological Science, 15(4), 555-559.
갤러리
2 장의 이미지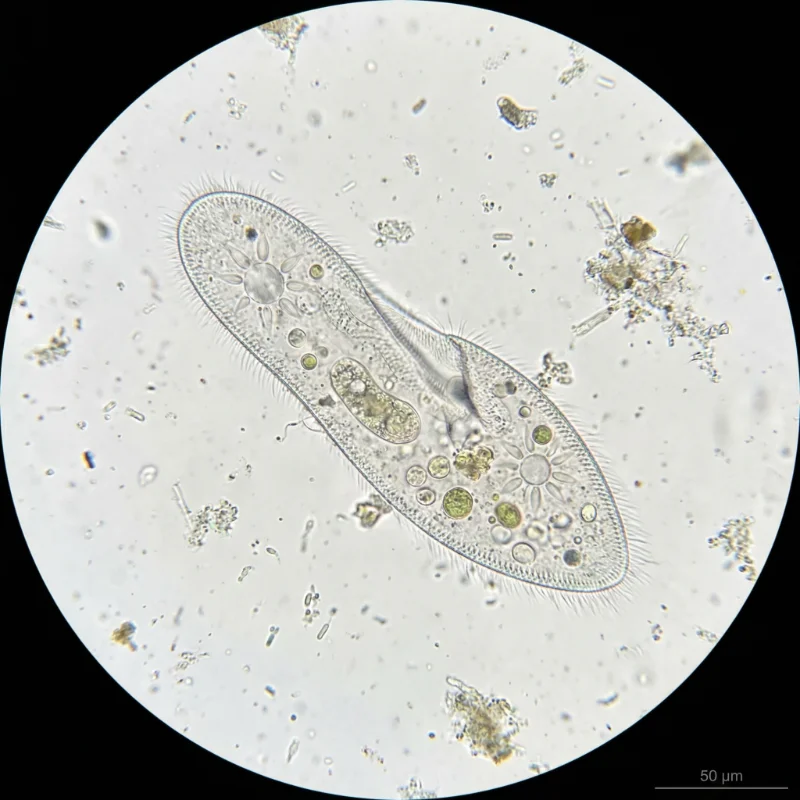 짚신벌레
짚신벌레짚신벌레
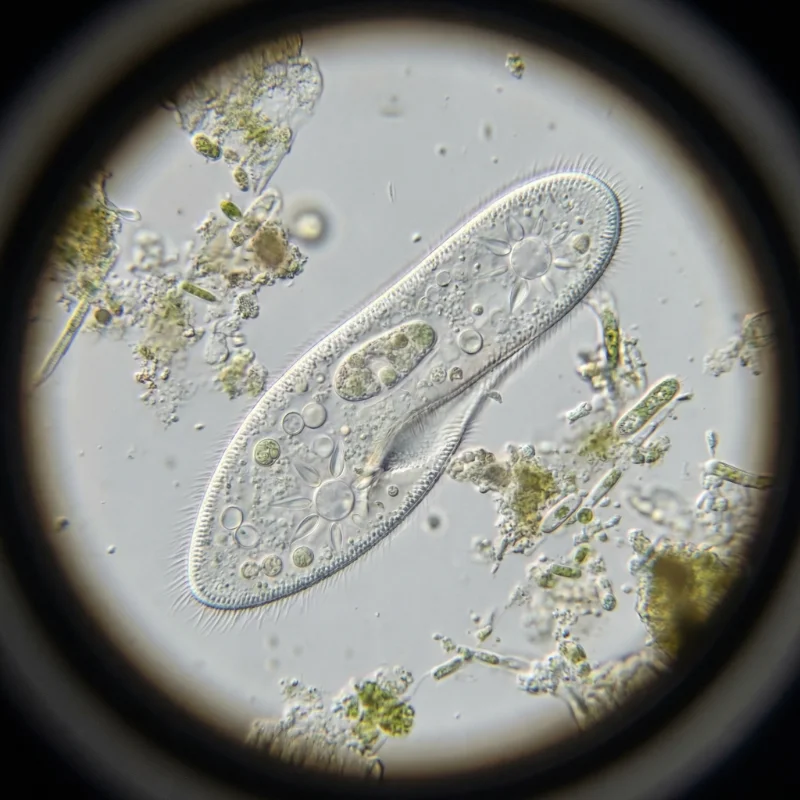 짚신벌레
짚신벌레짚신벌레