황색포도상구균
세균 · other
Staphylococcus aureus
학명 유래: "포도송이(staphyle, 그리스어) + 알갱이(kokkos, 그리스어) + 황금색(aureus, 라틴어)"
발견
미생물 특성
분류
서식지
분류 변천사
1880년 Alexander Ogston이 수술 후 농양에서 최초 관찰 및 Staphylococcus 속명 제안. 1884년 Friedrich Julius Rosenbach가 배양 집락 색상에 따라 S. aureus로 명명. 원래 Micrococcaceae 과에 분류되었으나, 분자계통학적 분석으로 독립 과인 Staphylococcaceae로 재분류. 1980년 Approved Lists of Bacterial Names에 등재. LPSN에서 정명(correct name) 및 의학적 권장명(LoRN) 유지
임상적 의미
피부·연조직 감염(SSTIs), 균혈증, 패혈증, 감염성 심내막염, 골수염, 폐렴, 식중독, 독소충격증후군(TSS) 등의 원인. MRSA는 전 세계 항생제 내성 관련 사망의 가장 치명적인 병원체-약제 조합(2021년 약 130,000명 직접 귀속 사망). WHO 항생제 내성 우선순위 병원체
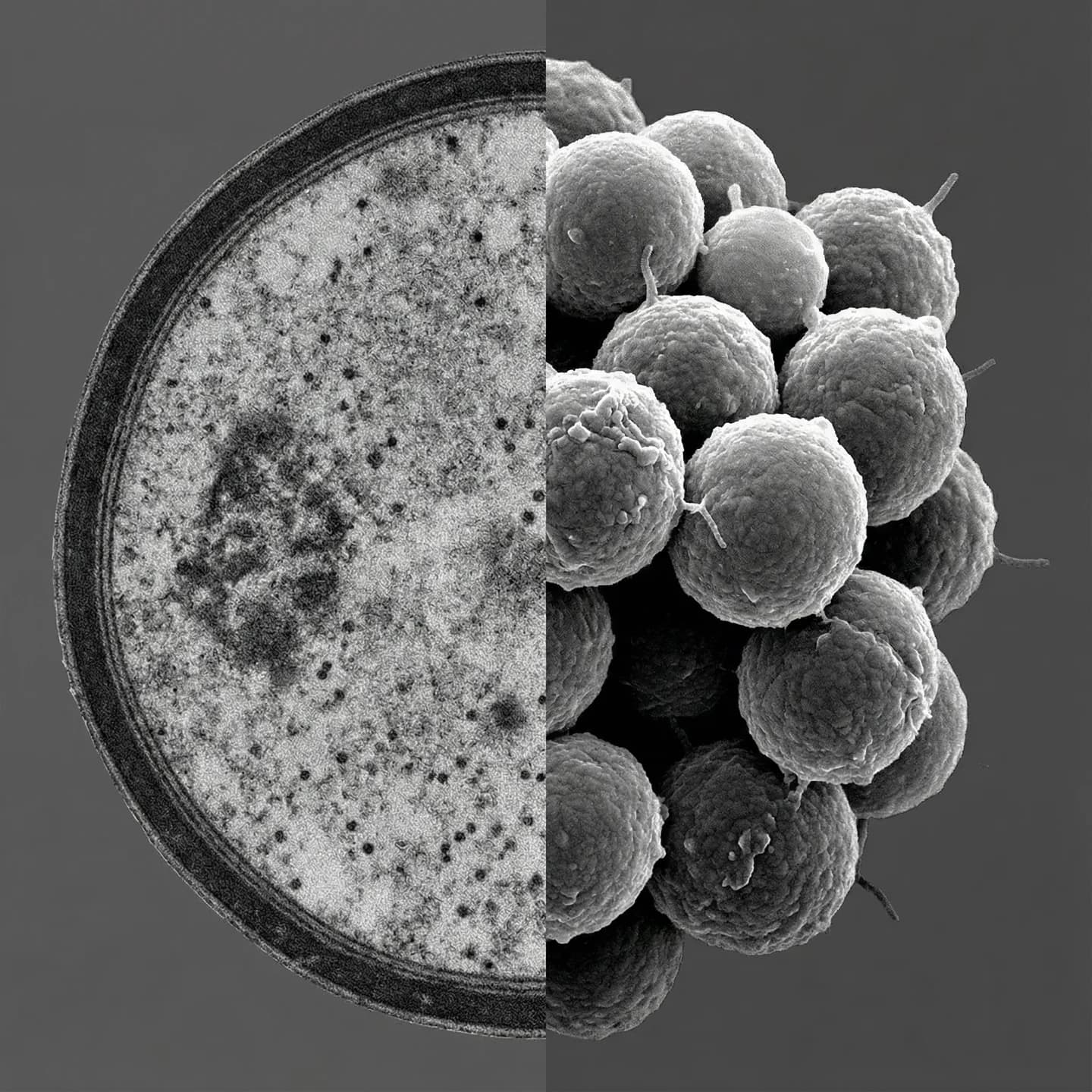
황색포도상구균(Staphylococcus aureus Rosenbach, 1884)은 포도상구균과(Staphylococcaceae) 포도상구균속(Staphylococcus)에 속하는 그람양성 구균으로, 인체 정상 미생물총(microbiota)의 일원이면서 동시에 가장 중요한 인체 병원균 중 하나이다. 직경 약 0.5~1.5 μm의 구형 세포가 포도송이 형태의 불규칙한 군집을 이루며, 배양 시 카로티노이드 색소인 스타필로잔틴(staphyloxanthin)의 생성으로 특징적인 황금색 집락(colony)을 형성한다. 통성 혐기성(facultative anaerobe)으로 산소 유무와 관계없이 성장할 수 있고, 카탈라제 양성·응고효소 양성이라는 생화학적 특성으로 다른 포도상구균 종과 구별된다. 유전체는 약 2.7~3.1 Mb 크기의 단일 원형 이중가닥 DNA 염색체로 구성되며, GC 함량은 약 32~33%이다. 생물안전등급(BSL)은 2등급으로 분류된다(CDC BMBL 6th Edition; LPSN Risk Group 2).
이 세균은 전체 인구의 약 20~30%의 비강에 지속적으로 집락화하며, 약 30%가 간헐적으로 보균한다(CDC, 2024). 정상 상태에서는 무증상 공생체로 존재하지만, 피부 장벽이 손상되거나 면역이 저하되면 경미한 피부 감염부터 치명적인 균혈증·패혈증·심내막염까지 광범위한 질환을 유발할 수 있는 '병원공생체(pathobiont)'이다. 세계보건기구(WHO)는 S. aureus를 항생제 내성 관련 가장 위협적인 병원체 중 하나로 지정하고 있으며, 특히 메티실린 내성 황색포도상구균(MRSA)은 전 세계적으로 가장 심각한 항생제 내성 문제의 핵심이다.
2024년 발표된 Global Burden of Disease(GBD) 2021 분석에 따르면, MRSA 관련 사망은 1990년 약 57,200명에서 2021년 약 130,000명으로 두 배 이상 증가했으며, MRSA와 연관된 사망은 같은 기간 261,000명에서 550,000명으로 급증했다(GBD 2021 AMR Collaborators, The Lancet, 2024). 미국에서는 연간 약 120,000건의 S. aureus 혈류 감염이 발생하며 약 20,000명이 사망하는 것으로 추정된다(CDC, 2019). 이처럼 S. aureus는 공중보건에 막대한 영향을 미치는 병원체로서, 현대 감염병학과 항생제 내성 연구의 중심에 놓여 있다.
1. 개요
속명 Staphylococcus는 그리스어 'σταφυλή(staphylē, 포도송이)'와 'κόκκος(kokkos, 알갱이/열매)'의 합성어로, 현미경 관찰 시 포도송이처럼 군집을 이루는 구균의 형태에서 유래했다. 종소명 aureus는 라틴어로 '황금색'을 의미하며, 배양 시 형성되는 황금색 집락 색상을 반영한다. 이 이름은 1884년 독일의 의사 Friedrich Julius Rosenbach가 집락 색상에 따라 황금색 균주를 S. aureus, 흰색 균주를 S. albus(현재 S. epidermidis)로 명명하면서 확립되었다.
현재 LPSN(List of Prokaryotic names with Standing in Nomenclature)에서 Staphylococcus aureus Rosenbach 1884는 유효 발표명(validly published name)이자 정명(correct name)으로 인정되며, 의학적으로 중요한 세균의 권장명 목록(LoRN)에도 등재되어 있다. S. aureus는 Staphylococcus속의 명명 기준종(nomenclatural type species)이다. NCBI Taxonomy에서의 분류 계통은 Bacteria > Bacillota(Firmicutes) > Bacilli > Bacillales > Staphylococcaceae > Staphylococcus > S. aureus이다.
S. aureus를 한 문장으로 요약하면, 인체의 가장 흔한 정상세균총 구성원 중 하나이면서 동시에 가장 치명적인 세균 병원체 중 하나라는 이중적 정체성을 가진 그람양성 구균이다.
2. 분류와 계통
분류학적 위치
S. aureus의 현재 분류학적 위치는 다음과 같다.
| 분류 단계 | 학명/명칭 |
|---|---|
| 역(Domain) | Bacteria |
| 문(Phylum) | Bacillota (동의어: Firmicutes) |
| 강(Class) | Bacilli |
| 목(Order) | Bacillales (동의어: Caryophanales) |
| 과(Family) | Staphylococcaceae |
| 속(Genus) | Staphylococcus |
| 종(Species) | S. aureus |
포도상구균속(Staphylococcus)은 원래 미구균과(Micrococcaceae)에 속하는 것으로 여겨졌으나, 분자계통학적 분석을 통해 미구균(Micrococcus)과 계통적으로 먼 관계임이 밝혀져 독립된 과인 포도상구균과(Staphylococcaceae)로 재분류되었다. 목(order) 수준에서는 NCBI Taxonomy 기준 Bacillales에 배치되어 있으나, USDA ACIR 등 일부 데이터베이스에서는 Caryophanales(Bacillales의 이시기 동의어)로 표기하는 경우도 있다.
명명 역사
1880년 스코틀랜드 Aberdeen의 외과의사 Alexander Ogston이 수술 후 농양에서 포도송이 형태의 세균 군집을 처음 관찰하고 Staphylococcus라는 속명을 제안했다. 그는 이 세균이 농양 형성의 원인임을 실험적으로 증명했다. 이후 1884년 독일의 Friedrich Julius Rosenbach가 배양 집락의 색상 차이에 근거하여 종 수준의 분류를 확립했다. Rosenbach는 원래 'Staphylococcus pyogenes aureus'로 명명했으나, 이후 종소명이 aureus로 간소화되었다. S. aureus는 1980년 Approved Lists of Bacterial Names(Skerman et al., 1980)에 등재되어 명명법적 유효성이 재확인되었다.
계통분석과 유전적 다양성
S. aureus의 계통 분류는 다좌위 서열형 분석(MLST, Multilocus Sequence Typing), spa 유형분석(spa typing), 전체 유전체 서열분석(WGS) 등 다양한 분자 타이핑 방법을 통해 이루어진다. MLST에 기반한 주요 클론 복합체(clonal complex)로는 CC1, CC5, CC8, CC15, CC22, CC30, CC45, CC97, CC398 등이 있으며, 이들은 각각 고유한 지리적 분포, 숙주 특이성, 항생제 내성 프로파일을 보인다.
CC8은 미국에서 가장 흔한 CA-MRSA 계통인 USA300을 포함하며, CC22(EMRSA-15)는 영국과 유럽에서 우세한 HA-MRSA 계통이다. CC398은 주로 가축(특히 돼지)에서 발견되는 가축 관련 MRSA(LA-MRSA) 계통으로, 축산업 종사자에게 전파될 수 있다. 약 10개의 주요 인간 계통이 인식되며, 균주 간 유전적 다양성이 크다.
주요 아종 및 변이
LPSN에 따르면 S. aureus에는 두 개의 유효 발표된 아종이 있다. S. aureus subsp. aureus(자동 생성된 기준 아종)와 S. aureus subsp. anaerobius(De La Fuente et al., 1985)가 있으며, 후자는 절대 혐기성으로 양(sheep)의 Morel 병을 유발한다.
항생제 감수성에 따른 주요 균주 분류로는 메티실린 감수성 황색포도상구균(MSSA), 메티실린 내성 황색포도상구균(MRSA), 반코마이신 중등도 내성 황색포도상구균(VISA, MIC 4~8 μg/mL), 반코마이신 내성 황색포도상구균(VRSA, MIC ≥16 μg/mL)이 있다. MRSA는 다시 병원 관련 MRSA(HA-MRSA), 지역사회 관련 MRSA(CA-MRSA), 가축 관련 MRSA(LA-MRSA)로 세분된다.
3. 형태와 구조
세포 형태
S. aureus는 직경 약 0.5~1.5 μm의 구형(coccus) 세균이다. 세포 분열 시 두 개의 수직 평면에서 교대로 분열하며, 딸세포가 완전히 분리되지 않아 포도송이 형태의 불규칙한 군집을 형성한다. 쌍(diplococci)이나 짧은 사슬(short chains), 단독 세포로도 관찰될 수 있다. 비운동성(nonmotile)이며, 내생포자(endospore)를 형성하지 않는다.
세포벽 구조
그람양성 세균으로서 두꺼운 펩티도글리칸(peptidoglycan) 층(약 20~30 nm)을 가진 세포벽을 보유하며, 그람염색에서 양성(보라색)으로 나타난다. 세포벽에는 벽 테이코산(wall teichoic acid, WTA)과 리포테이코산(lipoteichoic acid, LTA)이 풍부하게 존재하며, 이들은 세포벽 항상성, 자가용해, 항생제 내성, 숙주 세포 부착, 생물막 형성 등 다양한 기능에 관여한다. 외막(outer membrane)은 존재하지 않는다.
세포 표면에는 다양한 부착인자(adhesins)가 발현된다. 미생물 표면 구성 요소 인식 부착 기질 분자(MSCRAMMs, Microbial Surface Components Recognizing Adhesive Matrix Molecules)로 통칭되는 이 단백질들은 피브로넥틴, 피브리노겐, 콜라겐, 엘라스틴 등 숙주 세포외 기질 단백질에 결합하여 조직 부착과 감염 개시에 핵심적인 역할을 한다.
색소와 피막
S. aureus의 특징적인 황금색은 카로티노이드 색소인 스타필로잔틴(staphyloxanthin)에 의한 것이다. 스타필로잔틴은 항산화제로 기능하여 숙주 호중구가 생성하는 활성산소종(ROS, reactive oxygen species)으로부터 세균을 보호하며, 따라서 병원성 인자로도 작용한다. 일부 균주는 다당류 피막(capsule)을 생성하며, 혈청형(capsular polysaccharide type) 5형과 8형이 임상 분리주의 약 75~80%를 차지한다. 피막은 옵소닌화와 식균작용을 억제하여 면역 회피에 기여한다.
4. 유전체와 분자생물학
유전체 구조
S. aureus의 유전체는 단일 원형 이중가닥 DNA 염색체로 구성된다. NCBI RefSeq 데이터베이스에 등록된 다수의 기준 유전체를 종합하면, 유전체 크기는 약 2.7~3.1 Mb(메가염기쌍) 범위이며, 대표 균주(NCTC 8325 등)의 크기는 약 2.82 Mb이다. GC 함량은 약 32~33%로 비교적 낮다. 평균적으로 약 2,500~2,800개의 단백질 암호화 유전자를 포함하며, 이 중 약 56%가 핵심 유전체(core genome)를 구성한다.
이동성 유전 요소
유전체의 약 15~20%가 이동성 유전 요소(mobile genetic elements, MGEs)로 구성되며, 이는 S. aureus의 유전적 다양성과 적응력의 핵심 원천이다. 주요 이동성 유전 요소로는 박테리오파지(prophage), 병원성 섬(pathogenicity islands, SaPIs), 포도상구균 카세트 염색체(SCCmec), 삽입 서열(IS elements), 트랜스포존(transposons), 플라스미드(plasmids) 등이 있다.
SCCmec은 메티실린 내성 유전자 mecA(또는 변이형 mecC)를 운반하는 핵심 이동성 유전 요소로, 현재까지 14개 이상의 SCCmec 유형이 확인되었다. SCCmec 유형 I, II, III는 주로 HA-MRSA에서, 유형 IV, V는 CA-MRSA에서 발견된다. 병원성 섬은 독소 유전자(독소충격증후군 독소 TSST-1, 장독소 등)를 운반하며, 파지 매개 수평적 유전자 전달을 통해 균주 간 전파된다.
항생제 내성의 분자 기전
S. aureus의 항생제 내성 획득은 돌연변이와 수평적 유전자 전달(HGT)의 두 가지 메커니즘을 통해 이루어진다. 페니실린 내성은 blaZ 유전자에 의해 암호화되는 베타-락타마제(β-lactamase) 효소 생성을 통해 페니실린 고리를 가수분해하여 발생한다. 메티실린 내성은 mecA 유전자가 암호화하는 변형 페니실린 결합 단백질(PBP2a/PBP2')을 통해 매개되며, PBP2a는 베타-락탐 항생제에 대한 결합 친화력이 극히 낮아 세포벽 합성이 억제되지 않는다.
반코마이신 중등도 내성(VISA)은 세포벽 펩티도글리칸 두께의 증가와 D-Ala-D-Ala 잔기의 과잉 생산을 통해 반코마이신을 격리(sequestration)하는 메커니즘으로 발생한다. 반코마이신 완전 내성(VRSA)은 장구균(Enterococcus)으로부터 vanA 유전자 클러스터를 플라스미드 매개 접합(conjugation)으로 획득하여 세포벽 전구체의 말단을 D-Ala-D-Lac으로 변형함으로써 반코마이신 결합을 1,000배 이상 감소시킨다.
2022년 Nature에 발표된 연구(Eiamphungporn et al.)에 따르면, mecC 유전자에 의한 메티실린 내성의 기원은 항생제 사용 이전인 1940년대 중반까지 거슬러 올라가며, 피부사상균(Trichophyton spp.)에 감염된 유럽 고슴도치의 피부에서 S. aureus와 곰팡이 간의 공진화 과정에서 항진균 물질에 대한 자연 선택으로 발생한 것으로 추정된다.
5. 병원성과 임상 양상
감염 메커니즘
S. aureus의 감염은 일반적으로 부착(adhesion) → 침입(invasion) → 면역 회피(immune evasion) → 조직 손상(tissue damage)의 단계를 따른다. 부착 단계에서는 MSCRAMMs(피브로넥틴 결합 단백질 FnBPA/FnBPB, 응집인자 ClfA/ClfB, 콜라겐 결합 단백질 Cna 등)이 숙주 세포외 기질에 결합한다. 침입 단계에서는 피브로넥틴 결합 단백질이 인테그린 α5β1을 통해 비전문 식세포인 상피세포와 내피세포 내로 내재화(internalization)를 유도한다. 면역 회피 단계에서는 단백질 A(Protein A), 피막 다당류, 류코시딘, 보체 억제 단백질(SCIN, Efb, Ecb) 등이 작동한다.
독소와 효소
S. aureus는 다양한 독소를 분비하여 숙주 조직을 손상시킨다. 기공형성 독소(pore-forming toxins)로는 알파독소(α-hemolysin/Hla)가 숙주 세포막에 7량체 기공을 형성하여 세포를 용해시키며, 류코시딘(leukocidins)인 PVL(Panton-Valentine leucocidin), HlgAB/HlgCB, LukED, LukAB 등이 백혈구를 표적으로 파괴한다. 페놀용해성 모듈린(PSMs, phenol-soluble modulins)은 양친매성 α-나선 구조를 통해 세포막을 파괴하며 생물막 구조화, 세균 확산에도 관여한다.
초항원(superantigens)으로는 장독소(SE: SEA~SEE 등 20종 이상)와 독소충격증후군 독소-1(TSST-1)이 있다. 이들은 T세포 수용체(TCR)의 Vβ 영역과 MHC class II 분자에 동시에 결합하여 T세포의 비특이적 대량 활성화를 유발하고, 대량의 사이토카인(cytokine storm)을 방출시켜 전신성 염증 반응을 초래한다. 박리독소(exfoliative toxins, ETA/ETB)는 세린 프로테아제 활성을 가지며 데스모글레인 1(desmoglein 1)을 절단하여 표피 과립층을 분리시킨다.
주요 효소로는 응고효소(coagulase)와 폰 빌레브란트 인자 결합 단백질(vWbp)이 프로트롬빈을 활성화하여 피브린 응괴를 형성함으로써 세균을 면역계로부터 보호한다. 스타필로키나제(staphylokinase, SAK)는 플라스미노겐을 활성화하여 피브린 응괴를 용해하고 세균 확산을 촉진한다. DNA 분해효소(nuclease/DNase)는 호중구 세포외 덫(NETs, neutrophil extracellular traps)을 분해하여 면역 회피에 기여한다.
주요 질환
S. aureus가 유발하는 질환은 크게 세 범주로 나뉜다.
첫째, 피부 및 연조직 감염(SSTIs)이 가장 흔하며, 모낭염(folliculitis), 종기(furuncle/boil), 옹(carbuncle), 농가진(impetigo), 봉와직염(cellulitis), 농양(abscess) 등이 포함된다. CA-MRSA의 등장으로 건강한 젊은 성인에서도 중증 피부 감염이 증가했으며, PVL 양성 균주가 관여하는 경우가 많다.
둘째, 침습적 감염으로는 균혈증(bacteremia)과 패혈증(sepsis), 감염성 심내막염(infective endocarditis), 골수염(osteomyelitis), 패혈성 관절염(septic arthritis), 폐렴(pneumonia), 뇌농양, 경막외 농양 등이 있다. S. aureus 균혈증(SAB)의 발생률은 인구 100,000명당 연간 20~50건으로 추정되며, 30일 사망률은 15~30%에 이른다(Nature, 2025). MRSA 심내막염의 사망률은 30~37%로 매우 높다.
셋째, 독소 매개 질환으로는 식중독(장독소에 의한 급성 구역·구토, 잠복기 30분~8시간), 포도상구균성 화상피부증후군(SSSS, 주로 신생아·영유아), 독소충격증후군(TSS, TSST-1 또는 장독소에 의한 고열·발진·저혈압·다장기부전)이 있다.
생물막 형성
S. aureus는 의료 기기 표면에 생물막(biofilm)을 형성하는 능력이 뛰어나다. 생물막은 초기 부착(표면 단백질 매개), 축적(세포간 다당류 부착소 PIA/PNAG, 세포외 DNA, 단백질), 성숙, 분산(dispersal)의 4단계로 발달한다. 생물막 내부의 세균은 대사적으로 비활성화되어 항생제 최소억제농도(MIC)가 부유 세균 대비 10~1,000배 이상 증가하며, 면역 세포의 침투도 제한된다. 인공관절, 중심정맥 카테터, 심장 판막, 혈관 이식편, 정형외과 고정 기구 등에서 생물막 관련 감염이 빈발하며, 대부분 감염된 기기의 완전 제거가 필요하다.
6. 역학과 전파
인체 내 집락화
전비강(anterior nares)이 S. aureus의 가장 주요한 생태적 니치(ecological niche)이며, 인두(pharynx), 회음부, 겨드랑이, 서혜부, 피부(손, 가슴, 복부) 등도 주요 집락화 부위이다. CDC(2024)에 따르면 약 20~30%가 지속적 보균자(persistent carrier), 약 30%가 간헐적 보균자(intermittent carrier), 약 50%가 비보균자(non-carrier)로 분류된다. MRSA의 비강 보균율은 일반 인구의 약 2%로 추정된다(CDC, 2025). 비강 보균은 수술부위 감염, 균혈증, 복막투석 관련 감염 등 침습적 감염의 독립적 위험 인자로 확인되어 있다.
전파 경로와 역학
S. aureus의 전파는 직접 접촉(피부 대 피부), 간접 접촉(오염된 물체·표면), 비말 등을 통해 이루어진다. 병원 환경에서는 의료진의 손, 의료 기기, 침구류 등이 주요 전파 매개체이며, 원내 감염(nosocomial infection)의 5대 원인균 중 하나이다. 지역사회에서는 운동시설, 교정시설, 군사시설 등 밀접 접촉이 빈번한 환경에서 CA-MRSA 전파가 잘 일어난다.
전 세계적으로 MRSA의 유병률은 지역에 따라 큰 차이를 보인다. 2023년 발표된 메타분석에 따르면 전 세계 MRSA의 합산 유병률(pooled prevalence)은 약 14.7%(95% CI 12.4~17.2%)로 추정된다. GBD 2021 분석에 따르면 MRSA 관련 사망은 전 세계적으로 증가 추세에 있으며, 2021년 MRSA에 직접 귀속되는 사망이 약 130,000명, 연관 사망이 약 550,000명에 달한다(GBD 2021 AMR Collaborators, The Lancet, 2024).
동물 숙주
S. aureus는 반려동물(개, 고양이, 말), 가축(소, 돼지, 닭), 야생동물(고슴도치 등) 등 다양한 동물에서도 발견된다. 젖소에서 유방염(mastitis)의 주요 원인균으로 작용하며, 가축 관련 MRSA(LA-MRSA, 주로 CC398)는 축산업 종사자, 수의사 등에게 직업적 감염 위험을 초래한다. 인간과 반려동물 사이에서 양방향 전파가 확인되어 있다.
7. 면역·치료·예방
면역 반응
S. aureus에 대한 숙주 면역 반응은 선천면역이 주도적이다. 피부와 점막의 물리적 장벽, 항균 펩타이드(defensins, cathelicidins), 보체계(complement system)가 1차 방어선으로 작용한다. 호중구(neutrophils)는 S. aureus 감염에 대한 가장 핵심적인 선천면역 효과세포이며, 식균작용, 산화적 버스트(oxidative burst), 호중구 세포외 덫(NETs) 형성을 통해 세균을 제거한다. 적응면역에서는 항체 매개 면역(옵소닌화, 독소 중화)과 T세포(특히 Th17) 매개 면역이 모두 관여하나, S. aureus는 단백질 A, 피막 다당류, 보체 억제 단백질, 류코시딘, 초항원 등 다양한 기전으로 면역계를 회피한다.
항생제 치료
MSSA 감염의 표준 치료는 항포도상구균 페니실린(nafcillin, oxacillin) 또는 1세대 세팔로스포린(cefazolin)이며, 경증 피부 감염에는 세팔렉신(cephalexin) 또는 독시사이클린(doxycycline) 경구 투여가 사용된다.
MRSA 감염의 표준 1차 치료제는 반코마이신(vancomycin)이다. 대체 약물로는 답토마이신(daptomycin), 리네졸리드(linezolid), 테이코플라닌(teicoplanin), 트리메토프림-설파메톡사졸(TMP-SMX), 클린다마이신(clindamycin) 등이 있다. 2024년 메타분석(Ju et al., Int J Infect Dis)에 따르면 답토마이신이 MRSA 치료에 가장 높은 효과를 보였다. MRSA 폐렴에서는 리네졸리드가 폐 조직 침투력이 우수하여 선호된다. MRSA 균혈증에서는 반코마이신 또는 답토마이신이 권장되며, 감염원 제거(source control)가 필수적이다.
VISA/VRSA 감염은 답토마이신, 리네졸리드, 퀴누프리스틴-달포프리스틴(quinupristin-dalfopristin), 세프타롤린(ceftaroline, MRSA에 활성을 가진 5세대 세팔로스포린) 등을 활용하며, 감염 전문가의 상담이 권고된다.
탈집락화
수술 전 환자나 고위험 보균자에서 감염 예방을 위해 탈집락화(decolonization)가 시행된다. 일반적으로 무피로신(mupirocin) 2% 비강 연고를 5일간 1일 2회 도포하고, 클로르헥시딘(chlorhexidine) 4% 바디워시로 전신을 세정하는 프로토콜이 표준이다. 수술부위 감염 예방에 효과적인 것으로 입증되어 있다.
백신 개발
현재까지 S. aureus에 대한 승인된 백신은 없다. StaphVAX(Nabi Biopharmaceuticals), V710(Merck), SA4Ag(Pfizer) 등 여러 백신 후보가 임상 3상에서 효과를 입증하지 못했다. 백신 개발의 주요 장애물로는 S. aureus의 다양한 면역 회피 기전, 대부분의 사람이 이미 S. aureus에 노출되어 비보호적 면역 각인(non-protective immune imprinting)을 가지고 있다는 점, 체액성 면역과 세포성 면역을 모두 효과적으로 유도해야 한다는 점 등이 지목된다.
2024년 12월 UC San Diego 연구팀은 S. aureus가 면역 억제 단백질을 활성화하여 백신에 대한 면역 반응을 직접 저해한다는 메커니즘을 밝혀, 이를 차단함으로써 백신 효능을 회복시킬 수 있는 가능성을 동물 모델에서 제시했다(UC San Diego, 2024). 같은 달 스위스 LimmaTech Biologics의 다가 독소이드 백신 LBT-SA7이 미국 FDA로부터 패스트트랙(Fast Track) 지정을 받았으며, 2025년 2월 제1상 임상시험(NCT06719219)에 진입하여 최초 참가자 접종이 이루어졌다(CIDRAP, 2024; Contagion Live, 2025). 2025년 9월에는 5가지 핵심 독력인자를 표적으로 하는 다가 mRNA-LNP 칵테일 백신이 마우스 모델에서 우수한 효능을 입증한 결과가 npj Vaccines에 발표되었다.
8. 생태와 환경적 역할
환경 내 생존
S. aureus는 높은 환경 저항성을 가진다. 15%에 달하는 고농도 NaCl에서도 생존할 수 있어 염장 식품에서도 증식이 가능하며, 건조한 표면에서 수 주에서 수 개월간 생존할 수 있다. 이러한 특성은 병원 환경에서의 지속적 오염과 식품 오염에 직접적으로 기여한다. 최적 성장 온도는 30~37°C이나, 6~48°C 범위에서 생존할 수 있다. 배양 시 세대시간(doubling time)은 호기 조건에서 약 20~35분, 혐기 조건에서 약 80분이며, 인체 비강 내에서는 평균 1~3시간으로 추정된다(Krismer et al., 2019).
미생물 군집 내 상호작용
비강 내에서 S. aureus는 Corynebacterium spp., Dolosigranulum pigrum, S. epidermidis 등 다른 정상세균총과 경쟁적·협력적 상호작용을 한다. Corynebacterium 속 세균은 지질 분해를 통해 유리 지방산을 생성하고, 이는 S. aureus의 집락화를 억제하는 것으로 알려져 있다. S. lugdunensis가 생산하는 항생물질 루그두닌(lugdunin)은 S. aureus에 대해 강력한 항균 활성을 보여 프로바이오틱 기반 탈집락화 전략의 후보로 주목받고 있다.
식품 안전
S. aureus에 의한 식중독은 세균이 음식에서 증식하면서 생성한 장독소(enterotoxins)를 섭취하여 발생하는 중독형(intoxication) 식중독이다. 장독소는 100°C에서 30분간 가열해도 불활성화되지 않을 정도로 열에 안정적이다. 주로 사람이 직접 취급한 식품(샌드위치, 크림 소스, 유제품, 김밥 등)이 원인이 되며, 부적절한 온도 관리가 핵심 위험 요인이다.
9. 연구사와 과학적 의의
발견과 초기 연구
S. aureus의 발견사는 근대 세균학의 발전과 궤를 같이 한다. 1880년 Alexander Ogston이 수술 후 농양에서 포도송이 형태의 세균을 최초로 관찰하고, 마우스 모델을 통해 이 세균이 농양의 원인임을 증명했다. 이는 Koch의 감염병 병인론과 함께 세균이 특정 질병의 원인이라는 개념을 확립하는 데 기여했다. 1884년 Rosenbach의 분류로 종 수준의 명명이 이루어졌고, 이후 20세기 초에 걸쳐 응고효소, 용혈소 등 주요 독력인자가 순차적으로 발견되었다.
항생제 내성 연구의 모델
S. aureus는 항생제 내성 진화 연구의 대표적 모델 생물이다. 1940년대 페니실린 도입 직후 페니실리나제 생성 내성균이 출현했고, 1959년 메티실린 도입 후 1961년 영국에서 최초의 MRSA가 보고되었으며, 2002년 미국 미시간에서 최초의 VRSA가 분리되었다. 이러한 내성 출현의 역사는 항생제 사용과 내성 발달 사이의 군비 경쟁(arms race)을 생생하게 보여주는 사례이다.
현재 연구 동향
현재 S. aureus 연구의 주요 방향은 다음과 같다. 백신 개발에서는 다가 항원 전략, mRNA 기반 플랫폼, 면역 억제 메커니즘 극복 등이 활발히 탐구되고 있다. 대안적 치료법으로는 박테리오파지 치료(phage therapy), 항체 기반 치료(monoclonal antibodies), 항독력인자 전략(antivirulence strategies), 항생물막 제제 등이 연구 중이다. 역학적으로는 HA-MRSA와 CA-MRSA의 경계 모호화, LA-MRSA의 인간 전파 가능성, 전 세계적 항생제 내성 추이 모니터링 등이 주요 관심사이다.
10. 근연종 비교
| 특성 | S. aureus | S. epidermidis | S. saprophyticus | S. lugdunensis |
|---|---|---|---|---|
| 응고효소 | 양성 | 음성 | 음성 | 음성 |
| 용혈성 | 베타-용혈 | 비용혈/감마 | 비용혈/감마 | 베타-용혈 |
| 집락 색상 | 황금색 | 흰색/회색 | 흰색/노란색 | 크림색 |
| 주요 감염 | 피부, 폐렴, 패혈증, 심내막염 | 기기 관련 감염 | 요로 감염 | 심내막염, 피부 감염 |
| 병원성 | 높음 | 낮음(기회감염) | 낮음(요로 특이적) | 중간~높음 |
| 생물막 형성 | 높음 | 매우 높음 | 낮음 | 중간 |
| 주요 서식지 | 비강, 피부 | 피부 전신 | 비뇨생식기 | 회음부 |
| DNase | 양성 | 음성 | 음성 | 양성 |
S. epidermidis는 피부에서 가장 흔한 포도상구균으로, 일반적으로 비병원성이나 의료 기기(카테터, 인공판막 등)에 생물막을 형성하여 원내 감염을 유발할 수 있다. S. saprophyticus는 젊은 여성에서 요로 감염의 두 번째로 흔한 원인균이다. S. lugdunensis는 응고효소 음성이지만 S. aureus에 필적하는 병원성을 보일 수 있어 주의가 필요하며, 항생물질 루그두닌을 생산하여 S. aureus 집락화를 억제하는 것으로 알려져 있다.
재미있는 사실
메티실린 내성의 기원은 항생제 사용 이전인 1940년대까지 거슬러 올라간다. 2022년 Nature에 발표된 연구에 따르면, 피부사상균에 감염된 유럽 고슴도치의 피부에서 S. aureus와 곰팡이 간의 공진화 과정에서 항진균 물질에 대한 자연 선택으로 mecC 유전자가 발생한 것으로 밝혀졌다.
스타필로잔틴이라는 카로티노이드 색소가 S. aureus의 황금색을 만들어내는데, 이 색소는 단순한 색상이 아니라 면역 세포가 생성하는 활성산소를 중화시키는 '방패' 역할을 하는 병원성 인자이다.
최적 조건에서 S. aureus는 약 20분마다 분열할 수 있어, 이론적으로 단일 세포가 24시간 안에 약 10의 21승 개로 증가할 수 있다. 물론 실제로는 영양 고갈과 대사산물 축적으로 이보다 훨씬 적게 증식한다.
S. aureus의 장독소는 100°C에서 30분간 가열해도 파괴되지 않을 정도로 열에 안정적이어서, 오염된 음식을 충분히 조리해도 식중독을 예방할 수 없다. 처음부터 세균 오염을 방지하는 것이 유일한 대책이다.
S. aureus는 15%에 달하는 고농도 염분에서도 생존할 수 있으며, 건조한 표면에서 수 주에서 수 개월간 생존할 수 있다. 이러한 강인한 환경 저항성이 병원 내 지속 오염과 식품 안전 문제의 원인이다.
단백질 A는 S. aureus만의 독특한 면역 회피 무기로, 항체의 Fc 영역에 결합하여 항체를 '거꾸로' 붙게 만들어 옵소닌화와 보체 활성화를 무력화한다. 이 때문에 항체가 많아도 S. aureus를 효과적으로 제거하기 어렵다.
GBD 2021 분석에 따르면 MRSA에 직접 귀속되는 전 세계 사망이 2021년 약 130,000명으로, 1990년(약 57,200명)에 비해 두 배 이상 증가했다. MRSA는 단일 병원체-약제 조합으로서 항생제 내성 관련 가장 높은 사망 원인이다.
수십 년간의 집중적 연구에도 불구하고 S. aureus에 대한 효과적인 백신이 아직 없다. 2024년 UC San Diego 연구팀은 S. aureus가 면역 반응을 직접 억제하는 단백질을 활성화한다는 메커니즘을 밝혀, 반복된 백신 실패의 원인에 대한 새로운 단서를 제시했다.
응고효소(coagulase)를 생성하는 능력은 S. aureus를 다른 대부분의 포도상구균 종과 구별하는 핵심 특성이다. 이 효소는 프로트롬빈을 활성화하여 피브린 응괴로 세균을 감싸 면역 세포의 공격으로부터 보호하는 '은신처'를 만든다.
S. aureus는 사람뿐 아니라 반려동물(개, 고양이, 말)과 가축(소, 돼지)에서도 발견되며, 인간과 동물 사이에서 양방향 전파가 일어난다. 가축 관련 MRSA(LA-MRSA, CC398)는 축산업 종사자의 직업적 건강 위험으로 부상하고 있다.
2024년 12월, 스위스 LimmaTech Biologics의 다가 독소이드 백신 LBT-SA7이 미국 FDA 패스트트랙 지정을 받고 2025년 2월 제1상 임상시험에 진입했다. S. aureus에 대한 최초의 효과적인 백신 개발에 한 걸음 더 가까워진 것이다.
FAQ
황색포도상구균 보균자는 증상 없이 주로 비강이나 피부에 S. aureus가 존재하는 상태를 말합니다. CDC(2024)에 따르면 전체 인구의 약 20~30%가 지속적 보균자이고, 약 30%가 간헐적 보균자이며, 나머지 약 50%는 비보균자입니다. 보균 자체는 질병이 아니지만, 수술이나 피부 손상, 면역력 저하 시 감염으로 발전할 수 있으며, 다른 사람에게 전파될 수 있는 잠재적 감염원이 됩니다. 비강 보균은 수술부위 감염, 균혈증 등 침습적 감염의 독립적 위험 인자로 확인되어 있습니다.
증상은 감염 부위와 유형에 따라 다양합니다. 피부 감염은 발적, 부종, 통증, 농(고름)이 차는 종기나 농양으로 나타납니다. 식중독은 오염된 음식 섭취 후 30분~8시간 내에 구역, 구토, 복통, 설사가 급성으로 발생합니다. 침습적 감염으로는 고열, 오한(균혈증/패혈증), 호흡곤란과 기침(폐렴), 관절 통증과 부종(패혈성 관절염), 심장 이상(심내막염), 두통과 신경학적 증상(뇌농양) 등이 있으며, 패혈증으로 진행 시 다장기부전으로 생명을 위협할 수 있습니다. 독소충격증후군은 갑작스러운 고열, 발진, 저혈압, 다장기부전을 특징으로 합니다.
지역사회에서의 주요 예방법으로는 비누와 물로 손을 자주 씻거나 알코올 손소독제를 사용하는 것, 상처를 깨끗하고 건조하게 유지하며 붕대로 덮는 것, 수건·면도기·운동복 등 개인 물품을 공유하지 않는 것, 운동기구 등 공용 표면을 사용 전후 닦는 것 등이 있습니다. 의료 환경에서는 철저한 손위생, 접촉 격리(가운·장갑 착용), 환경 표면 소독, 고위험 환자 대상 MRSA 선별검사(능동적 감시), 수술 전 무피로신/클로르헥시딘을 이용한 탈집락화 등이 시행됩니다.
현재까지 S. aureus에 대한 승인된 백신은 없습니다. StaphVAX, V710, SA4Ag 등 여러 백신 후보가 임상시험에서 효과를 입증하지 못했습니다. 그러나 2024년 12월 LimmaTech Biologics의 다가 독소이드 백신 LBT-SA7이 미국 FDA 패스트트랙 지정을 받고 2025년 2월 제1상 임상시험에 진입했으며, mRNA 기반 다가 백신 등 새로운 플랫폼을 활용한 후보들이 전임상 단계에서 유망한 결과를 보이고 있습니다. S. aureus의 다양한 면역 회피 기전과 비보호적 면역 각인(non-protective immune imprinting)을 극복하는 것이 백신 개발의 핵심 과제입니다.
S. aureus 식중독은 감염형이 아닌 중독형(intoxication) 식중독입니다. 세균이 음식에서 증식하면서 이미 생성한 장독소(enterotoxin)를 섭취하여 발생하므로, 체내에서 세균이 증식할 시간이 필요 없어 잠복기가 30분~8시간으로 매우 짧습니다. 또한 장독소는 100°C에서 30분간 가열해도 파괴되지 않을 정도로 열에 안정적이어서, 오염된 음식을 충분히 조리해도 식중독을 예방할 수 없습니다. 따라서 식품 취급 시 위생 관리와 적절한 냉장 보관(5°C 이하)으로 세균 증식을 처음부터 방지하는 것이 핵심입니다.
S. aureus는 의료 기기 표면에 생물막(biofilm)을 형성하는 능력이 뛰어납니다. 체내 삽입된 기기 표면이 숙주 단백질(피브리노겐, 피브로넥틴 등)로 코팅되면 MSCRAMMs 등 부착인자를 통해 강하게 결합합니다. 이후 세포간 다당류 부착소(PIA/PNAG), 세포외 DNA, 단백질로 구성된 세포외 기질을 생성하여 성숙한 생물막을 형성합니다. 생물막 내부의 세균은 항생제 침투가 어렵고(MIC가 10~1,000배 증가), 대사적으로 비활성 상태여서 항생제의 표적이 되기 어려우며, 면역 세포의 접근도 제한됩니다. 이 때문에 대부분 감염된 기기를 완전히 제거해야 치료가 가능합니다.
황금색은 스타필로잔틴(staphyloxanthin)이라는 카로티노이드 색소에 의한 것입니다. 이 색소는 단순한 외관상 특징만이 아니라 중요한 병원성 인자로 작용합니다. 스타필로잔틴은 세포막에 위치하여 항산화 작용을 통해 숙주 호중구가 산화적 버스트(oxidative burst)로 생성하는 활성산소종(ROS)과 싱글렛 산소(singlet oxygen)를 중화시켜 세균의 세포 내 생존을 도와줍니다. 스타필로잔틴 합성이 억제된 돌연변이 균주는 호중구에 의해 더 쉽게 사멸되며, 이는 이 색소가 면역 회피에 직접 기여함을 보여줍니다.
MRSA 감염 증가의 주요 요인은 다층적입니다. 항생제의 과잉·부적절 사용이 내성 균주의 선택적 이점을 부여하여 확산을 촉진합니다. 병원 환경에서의 교차 감염(의료진의 손, 오염된 의료 기기 등)이 HA-MRSA 전파의 핵심 경로이며, 1990년대 이후 CA-MRSA가 출현하면서 건강한 지역사회 구성원에게도 감염이 확산되었습니다. 축산업에서의 항생제 사용으로 LA-MRSA(주로 CC398)가 가축에서 증가하여 인간에게도 전파됩니다. GBD 2021 분석에 따르면 MRSA 관련 사망은 1990~2021년 사이 두 배 이상 증가했습니다.
예, S. aureus는 사람과 반려동물(개, 고양이, 말 등) 사이에서 양방향으로 전파될 수 있습니다. 반려동물은 주인으로부터 S. aureus(MRSA 포함)에 감염될 수 있으며, 감염된 반려동물이 다시 사람에게 전파원이 될 수 있습니다. 특히 가축(돼지, 소)과 밀접하게 접촉하는 축산업 종사자와 수의사에서 LA-MRSA(CC398) 보균이 빈번합니다. 이러한 동물-인간 간 전파(zoonotic transmission)는 MRSA 역학의 중요한 측면이며, One Health 관점에서의 감시가 필요합니다.
📚참고문헌
- Rosenbach FJ. Mikroorganismen bei den Wund-Infections-Krankheiten des Menschen. J.F. Bergmann, Wiesbaden, 1884.
- Ogston A. Report upon micro-organisms in surgical diseases. British Medical Journal. 1881;1(1054):369-375. https://doi.org/10.1136/bmj.1.1054.369.b
- Tong SY, Davis JS, Eichenberger E, Holland TL, Fowler VG Jr. Staphylococcus aureus infections: epidemiology, pathophysiology, clinical manifestations, and management. Clinical Microbiology Reviews. 2015;28(3):603-661. https://doi.org/10.1128/CMR.00134-14
- Lowy FD. Staphylococcus aureus infections. New England Journal of Medicine. 1998;339(8):520-532. https://doi.org/10.1056/NEJM199808203390806
- GBD 2019 Antimicrobial Resistance Collaborators. Global burden of bacterial antimicrobial resistance in 2019: a systematic analysis. The Lancet. 2022;399(10325):629-655. https://doi.org/10.1016/S0140-6736(21)02724-0
- GBD 2021 Antimicrobial Resistance Collaborators. Global burden of bacterial antimicrobial resistance 1990–2021: a systematic analysis with forecasts to 2050. The Lancet. 2024;404(10459):1199-1226. https://doi.org/10.1016/S0140-6736(24)01867-1
- CDC. Vital Signs: Epidemiology and Recent Trends in Methicillin-Resistant Staphylococcus aureus Bloodstream Infections. MMWR Morb Mortal Wkly Rep. 2019;68(9):214-219. https://www.cdc.gov/mmwr/volumes/68/wr/mm6809e1.htm
- CDC. Staphylococcus aureus Basics. Centers for Disease Control and Prevention. 2024. https://www.cdc.gov/staphylococcus-aureus/about/index.html
- Eiamphungporn W, Schauss AC, Heine D, et al. Emergence of methicillin resistance predates the clinical use of antibiotics. Nature. 2022;602:135-141. https://doi.org/10.1038/s41586-021-04265-w
- Foster TJ. Antibiotic resistance in Staphylococcus aureus. Current status and future prospects. FEMS Microbiology Reviews. 2017;41(3):430-449. https://doi.org/10.1093/femsre/fux007
- Wertheim HF, Melles DC, Vos MC, et al. The role of nasal carriage in Staphylococcus aureus infections. The Lancet Infectious Diseases. 2005;5(12):751-762. https://doi.org/10.1016/S1473-3099(05)70295-4
- Otto M. MRSA virulence and spread. Cellular Microbiology. 2012;14(10):1513-1521. https://doi.org/10.1111/j.1462-5822.2012.01832.x
- Krismer B, Abt C, Taxis K, et al. Rapid cell division of Staphylococcus aureus during colonization of the human nose. mBio. 2019;10(2):e00285-19. https://doi.org/10.1128/mBio.00285-19
- Liu C, Bayer A, Cosgrove SE, et al. Clinical Practice Guidelines by the Infectious Diseases Society of America for the Treatment of Methicillin-Resistant Staphylococcus aureus Infections in Adults and Children. Clinical Infectious Diseases. 2011;52(3):e18-e55. https://doi.org/10.1093/cid/ciq146
- Ju G, Han Y, Chen J, et al. Comparative effectiveness and safety of six antibiotics in treating MRSA infections: a network meta-analysis. International Journal of Infectious Diseases. 2024;145:107076. https://doi.org/10.1016/j.ijid.2024.107076
- WHO. Global Priority List of Antibiotic-Resistant Bacteria to Guide Research, Discovery, and Development of New Antibiotics. World Health Organization. 2017.
- Skerman VBD, McGowan V, Sneath PHA. Approved lists of bacterial names. International Journal of Systematic Bacteriology. 1980;30:225-420.
- LimmaTech Biologics. FDA Fast Track Designation for LBT-SA7. Press Release. December 19, 2024. https://lmtbio.com
- CDC/NIH. Biosafety in Microbiological and Biomedical Laboratories (BMBL), 6th Edition. 2020. https://www.cdc.gov/labs/pdf/SF__19_308133-A_BMBL6_00-BOOK-WEB-final-3.pdf
갤러리
4 장의 이미지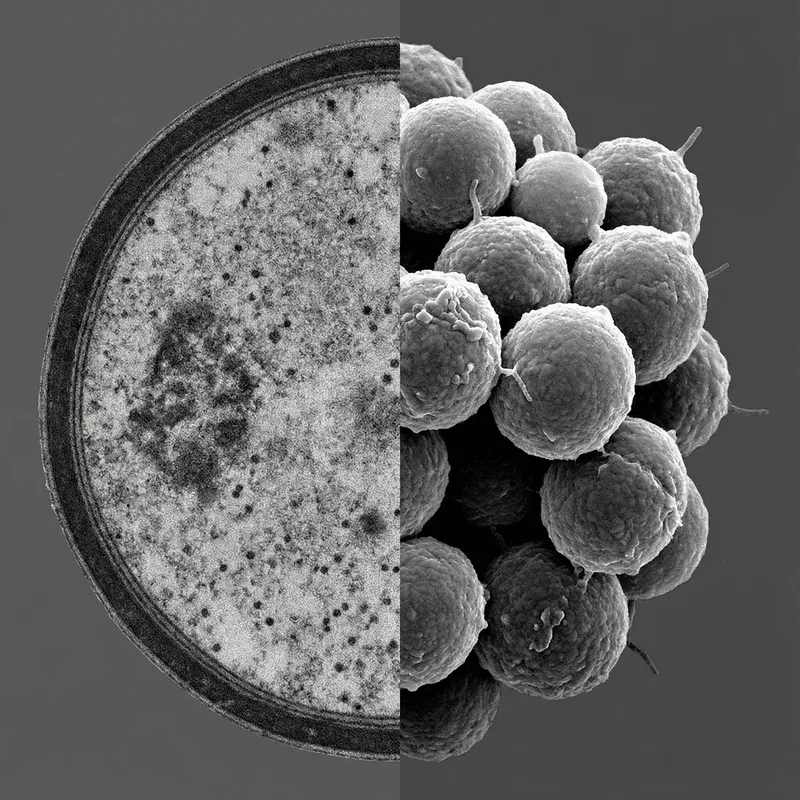 황색포도상구균
황색포도상구균황색포도상구균
 황색포도상구균
황색포도상구균황색포도상구균
 황색포도상구균
황색포도상구균황색포도상구균
 황색포도상구균
황색포도상구균황색포도상구균