인플루엔자 바이러스
바이러스 · other
Influenzavirus A, B, C, D
학명 유래: "라틴어 'influentia'(영향)에서 유래, 중세 시대 질병이 별들의 점성학적 영향에 의해 발생한다는 믿음에서 기원. 그리스어 'myxa'(점액)와 'orthos'(올바른)를 결합한 Orthomyxoviridae과 명칭은 바이러스가 점막에 친화성을 가짐을 반영"
발견
미생물 특성
분류
서식지
분류 변천사
1933년 Smith, Andrewes, Laidlaw가 인간 인플루엔자 바이러스 최초 분리. 이후 1940년 B형, 1947년 C형 발견. 2011년 D형 최초 확인. ICTV에 의해 Orthomyxoviridae과 하 4개 속으로 분류. 2021~2023년 ICTV 이명법 의무화에 따라 종명이 binomial format으로 재명명(예: Alphainfluenzavirus influenzae)
임상적 의미
계절성 인플루엔자 원인체(연간 전 세계 약 10억 감염, 29만~65만 사망). 팬데믹 유발 가능(1918 스페인 독감, 2009 신종플루 등). 고병원성 조류 인플루엔자 H5N1의 인수공통감염 위험 지속

인플루엔자 바이러스(Influenzavirus)는 오르토믹소바이러스과(Orthomyxoviridae)에 속하는 분절형 음성 단일가닥 RNA 바이러스(negative-sense single-stranded segmented RNA virus)로, 인간과 다양한 동물에서 급성 호흡기 감염을 일으키는 주요 병원체이다. 국제바이러스분류위원회(ICTV)의 현행 분류에 따라 인플루엔자 A, B, C, D의 네 가지 유형이 각각 알파인플루엔자바이러스속(Alphainfluenzavirus), 베타인플루엔자바이러스속(Betainfluenzavirus), 감마인플루엔자바이러스속(Gammainfluenzavirus), 델타인플루엔자바이러스속(Deltainfluenzavirus)으로 분류되어 있다. 2023년부터 ICTV의 이명법(binomial nomenclature) 의무화에 따라 종명은 각각 Alphainfluenzavirus influenzae, Betainfluenzavirus influenzae, Gammainfluenzavirus influenzae, Deltainfluenzavirus influenzae로 재명명되었다.
세계보건기구(WHO)에 따르면 전 세계적으로 매년 약 10억 건의 계절성 인플루엔자 감염이 발생하며, 이 중 300만~500만 건이 중증으로 발전하고, 약 29만~65만 명이 호흡기 관련 사망에 이른다(WHO, 2025). 미국 CDC의 추산에 따르면 2024~2025 시즌에는 약 5,100만 건의 인플루엔자 질환, 71만 건의 입원, 4만 5,000명의 사망이 발생하여 높은 중증도의 시즌으로 기록되었다(CDC, 2026). 개발도상국에서 5세 미만 아동의 인플루엔자 관련 하기도 감염 사망의 99%가 발생한다.
"인플루엔자(Influenza)"라는 명칭은 라틴어 "influentia"에서 유래하였으며, 중세 시대에 이 질병이 별들의 점성학적 "영향(influence)"에 의해 발생한다고 믿었던 것에서 비롯되었다. 과(科) 명칭인 "Orthomyxoviridae"는 그리스어 'myxa'(점액)와 'orthos'(올바른, 정확한)의 조합으로, 바이러스가 점막에 친화성을 가짐을 반영한다. 1933년 영국의 윌슨 스미스(Wilson Smith), 크리스토퍼 앤드류스(Christopher Andrewes), 패트릭 레이들로(Patrick Laidlaw)가 인간에서 최초로 인플루엔자 바이러스를 분리하였으며, 이에 앞서 1931년 리처드 쇼프(Richard Shope)가 돼지에서 인플루엔자 바이러스를 분리한 바 있다.
1. 개요
인플루엔자 바이러스는 인류가 직면한 가장 중요한 호흡기 바이러스 병원체 중 하나로, 계절성 유행과 불규칙적인 팬데믹을 통해 지속적인 공중보건 위협을 가한다. Baltimore 분류 체계에서 Group V(음성 단일가닥 RNA 바이러스)에 해당하며, 분절형 유전체를 통한 재배열(reassortment) 능력이 팬데믹 잠재력의 핵심적 기반이다. 계절성 인플루엔자 백신은 가장 효과적인 예방 수단이지만, 바이러스의 지속적인 항원 변이로 인해 매년 백신 조성을 갱신해야 한다.
현재 인간에서 계절적으로 순환하는 인플루엔자 바이러스는 A(H1N1)pdm09, A(H3N2), 그리고 B/Victoria 계통이다. B/Yamagata 계통은 COVID-19 팬데믹 기간의 비약물적 중재 조치로 인해 2020년 3월 이후 전 세계적으로 검출되지 않고 있으며, 이에 따라 2025~2026 시즌부터 모든 인플루엔자 백신은 3가(trivalent) 구성으로 전환되었다(CDC, 2026; WHO, 2025). 한편 고병원성 조류 인플루엔자 A(H5N1)는 2024년 미국 젖소 농장 발생 이후 동물-인간 접점에서의 산발적 인간 감염이 지속 보고되어, 차세대 팬데믹에 대한 경계가 높아지고 있다.
2. 분류와 계통
인플루엔자 바이러스의 분류학적 위치는 다음과 같다.
| 분류 단계 | 학명/명칭 |
|---|---|
| 역(Realm) | Riboviria |
| 계(Kingdom) | Orthornavirae |
| 문(Phylum) | Negarnaviricota |
| 아문(Subphylum) | Polyploviricotina |
| 강(Class) | Insthoviricetes |
| 목(Order) | Articulavirales |
| 과(Family) | Orthomyxoviridae |
| 속(Genus) | Alphainfluenzavirus (A형), Betainfluenzavirus (B형), Gammainfluenzavirus (C형), Deltainfluenzavirus (D형) |
ICTV는 2021년 모든 바이러스 종명에 대해 이명법(binomial nomenclature)을 의무화하기 시작하였으며, 이에 따라 기존의 "Influenza A virus"는 Alphainfluenzavirus influenzae로, "Influenza B virus"는 Betainfluenzavirus influenzae로 재명명되었다. 이 변경은 2023년에 NCBI Taxonomy에 반영되었다(NCBI Insights, 2023). 오르토믹소바이러스과에는 인플루엔자 바이러스 4개 속 외에도 토고토바이러스속(Thogotovirus), 콰란자바이러스속(Quaranjavirus), 이사바이러스속(Isavirus) 등이 포함되어 있다.
인플루엔자 A 바이러스(Alphainfluenzavirus influenzae)는 가장 중요한 인플루엔자 유형으로, 인간에서 계절성 유행과 팬데믹을 모두 일으킬 수 있다. 표면 단백질인 헤마글루티닌(HA)과 뉴라미니데이스(NA)의 조합에 따라 아형(subtype)으로 분류되며, 현재까지 18종의 HA 아형(H1~H18)과 11종의 NA 아형(N1~N11)이 확인되었다. 인간에서 계절적으로 순환하는 주요 아형은 A(H1N1)과 A(H3N2)이다. 야생 수금류가 인플루엔자 A 바이러스의 자연 저장숙주로, 거의 모든 HA와 NA 아형 조합이 조류에서 발견된다.
인플루엔자 B 바이러스(Betainfluenzavirus influenzae)는 주로 인간에만 감염되며, 아형으로 분류되지 않고 계통(lineage)으로 구분된다. B/Victoria 계통과 B/Yamagata 계통 두 가지가 존재하였으나, B/Yamagata 계통은 2020년 3월 이후 전 세계적으로 검출되지 않고 있어 사실상 소멸(probable extinction)한 것으로 판단된다(Caini et al., Lancet Microbe, 2024). COVID-19 팬데믹 기간의 비약물적 중재 조치(마스크 착용, 사회적 거리두기, 여행 제한 등)가 순환 감소의 주요 원인으로 분석되며, B/Victoria는 이후 재유행하였으나 B/Yamagata는 복귀하지 못하였다. 이에 따라 2025~2026 시즌부터 모든 인플루엔자 백신은 B/Yamagata를 제외한 3가(trivalent) 백신으로 전환되었다(FDA, 2025; WHO, 2025). 인플루엔자 B는 A보다 유전적, 항원적 변이 속도가 느리며, 동물 저장숙주가 없어 팬데믹을 일으키지 않는다.
인플루엔자 C 바이러스(Gammainfluenzavirus influenzae)는 인간과 돼지에 감염되며, 경증의 상기도 감염이나 무증상 감염을 일으킨다. 유전체가 7개 분절로 구성되어 A형, B형의 8개 분절보다 적으며, HA와 NA 대신 헤마글루티닌-에스터라제-융합(HEF) 단백질 하나가 두 기능을 모두 수행한다. 계절성 유행이나 팬데믹을 일으키지 않으며, 공중보건적 중요성은 낮다.
인플루엔자 D 바이러스(Deltainfluenzavirus influenzae)는 2011년에 처음 확인된 가장 최근에 발견된 유형으로, 주로 소와 돼지에 감염된다. 인간에서의 감염은 드물지만, 소에 노출되는 축산업 종사자에서 혈청학적 양성이 보고된 바 있다. 인플루엔자 C와 마찬가지로 7개의 유전체 분절을 가지며, 인간에서 질병을 일으키는 능력은 현재까지 확인되지 않았다.
3. 형태와 구조
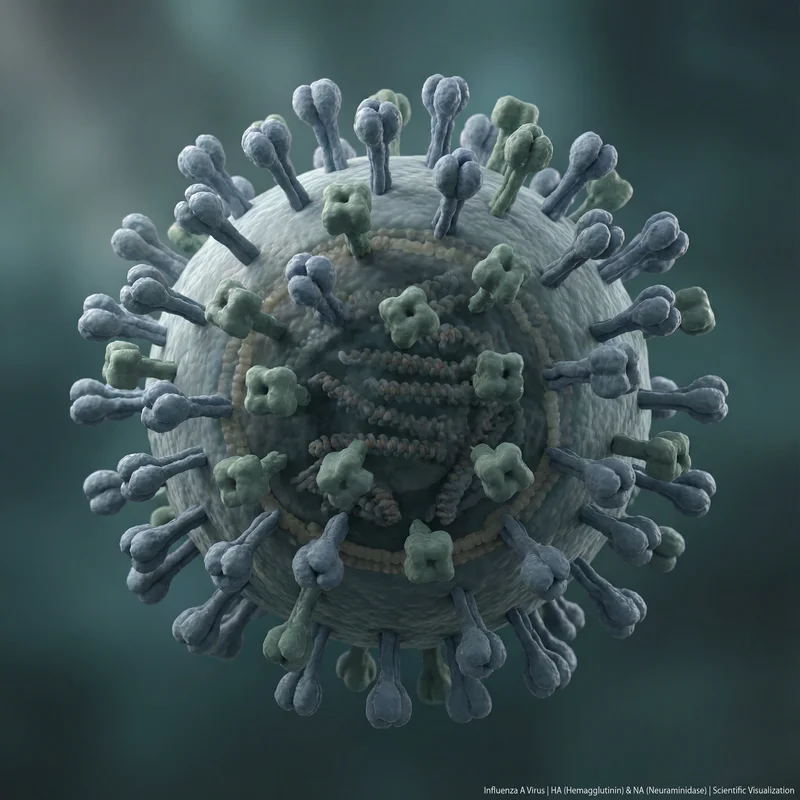
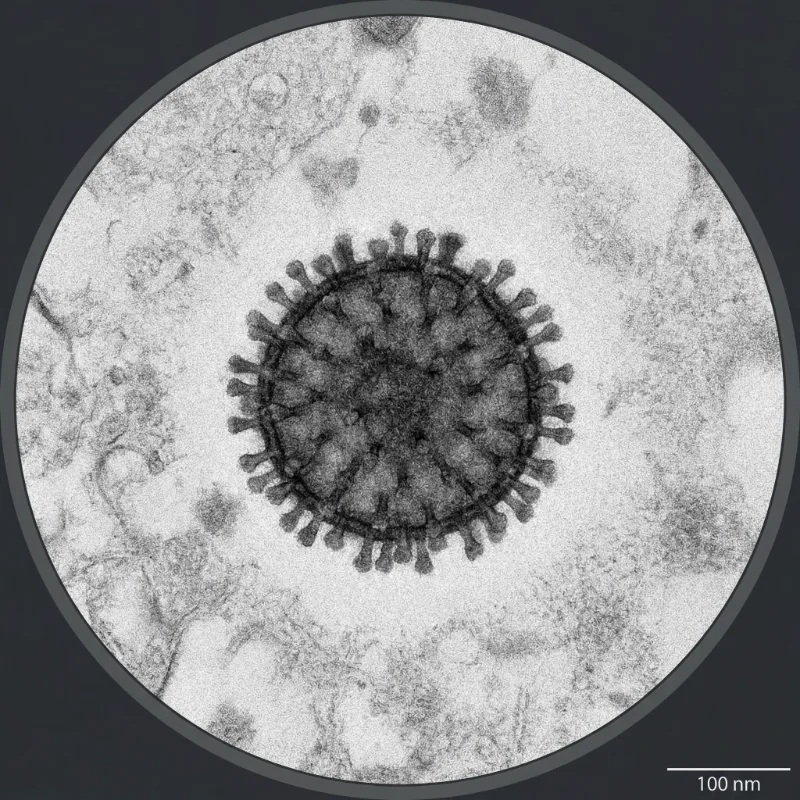
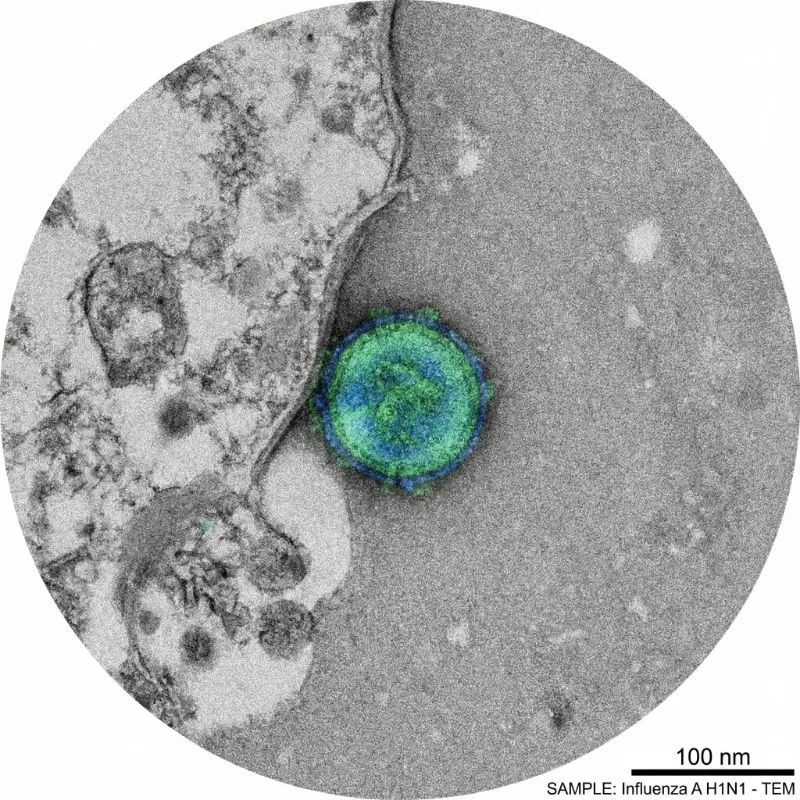
인플루엔자 바이러스는 다형성(pleomorphic) 외피 바이러스로, 구형과 사상형(filamentous) 두 가지 형태로 존재한다. 구형 비리온의 직경은 약 80~120nm이며, 사상형은 직경 약 80nm에 길이가 300nm에서 수 μm에 달할 수 있다. 실험실 적응 주는 주로 구형이지만, 임상 분리주는 사상형이 더 흔하다. 바이러스 표면에는 HA와 NA 스파이크가 약 7~14nm 높이로 돌출되어 있으며, HA가 NA보다 약 4~5배 많다.
헤마글루티닌(HA)은 바이러스 표면에서 가장 풍부한 당단백질(약 500개/비리온)로, 삼량체(trimer) 형태로 존재한다. HA는 숙주세포 표면의 시알산(sialic acid) 수용체에 결합하여 바이러스 침입을 개시하고, 엔도좀 산성화 시 막융합을 매개한다. HA는 HA1(수용체 결합 영역)과 HA2(융합 영역)로 구성되며, 숙주 프로테아제에 의한 절단이 감염력 활성화에 필수적이다.
뉴라미니데이스(NA)는 사량체(tetramer) 형태의 효소 당단백질로, 시알산을 절단하여 새로 형성된 바이러스가 숙주세포에서 방출되도록 돕고, 점액층 통과를 촉진한다. NA는 오셀타미비르(타미플루), 자나미비르(렐렌자) 등 항바이러스제의 표적이다.
M1(매트릭스 1) 단백질은 바이러스 외피 내면에 층을 형성하여 구조적 안정성을 제공하며, 비리온 조립과 출아에 핵심적인 역할을 한다. M2 단백질은 사량체 양성자 이온 채널로, 바이러스 탈피 과정에서 엔도좀 산성화를 비리온 내부로 전달하여 M1-vRNP 해리를 촉진한다. NS1 단백질은 숙주의 인터페론 반응을 억제하는 주요 병독성 인자이며, NEP(NS2)는 vRNP의 핵에서 세포질로의 수송을 담당한다.
4. 유전체와 분자생물학
인플루엔자 A와 B 바이러스는 8개의 분절로 구성된 음성 단일가닥 RNA 유전체를 가지며, 인플루엔자 C와 D는 7개 분절을 가진다. 전체 유전체 크기는 약 13.5kb(A형, B형)이다. 각 RNA 분절은 바이러스 리보뉴클레오단백질 복합체(vRNP) 형태로 존재하며, 뉴클레오캡시드 단백질(NP)과 RNA의존RNA중합효소(RdRp) 복합체(PB1, PB2, PA)와 결합해 있다.
인플루엔자 A 바이러스의 8개 RNA 분절은 다음과 같은 단백질을 암호화한다.
| 분절 | 크기 (nt) | 주요 단백질 | 기능 |
|---|---|---|---|
| 1 (PB2) | 약 2,341 | PB2 | RNA 중합효소 소단위, 캡 결합 |
| 2 (PB1) | 약 2,341 | PB1, PB1-F2 | RNA 중합효소 소단위, 세포자멸사 유도 |
| 3 (PA) | 약 2,233 | PA, PA-X | RNA 중합효소 소단위, 엔도뉴클레이스 활성 |
| 4 (HA) | 약 1,778 | HA (헤마글루티닌) | 수용체 결합, 막융합 |
| 5 (NP) | 약 1,565 | NP (뉴클레오단백질) | vRNA 결합, vRNP 구조 형성 |
| 6 (NA) | 약 1,413 | NA (뉴라미니데이스) | 시알산 절단, 바이러스 방출 |
| 7 (M) | 약 1,027 | M1, M2 | 매트릭스 단백질, 이온 채널 |
| 8 (NS) | 약 890 | NS1, NEP/NS2 | 인터페론 길항제, vRNP 핵외수송 |
인플루엔자 바이러스의 복제 주기는 다음 단계로 구성된다. 첫째, 부착(attachment) 단계에서 HA가 숙주세포 표면의 시알산 수용체에 결합한다. 인간 적응 바이러스는 α2,6-시알산 연결을, 조류 적응 바이러스는 α2,3-시알산 연결을 선호한다. 둘째, 수용체 매개 세포내섭취(receptor-mediated endocytosis)를 통해 바이러스가 엔도좀으로 내포화된다. 셋째, 엔도좀의 산성화(pH ~5)가 HA의 구조 변화를 유발하여 바이러스 외피와 엔도좀 막의 융합을 촉발하고, 동시에 M2 이온 채널이 양성자를 유입시켜 vRNP가 방출된다. 넷째, vRNP가 핵으로 이동하여 바이러스 RNA 전사와 복제가 핵 내에서 이루어진다. 다섯째, 바이러스 mRNA가 세포질에서 번역되고, 새로운 vRNP가 형성되어 핵에서 수송된다. 마지막으로 바이러스 단백질과 vRNP가 세포막에서 조립되고, NA가 시알산을 절단하여 새 비리온이 출아(budding)한다.
인플루엔자 바이러스의 돌연변이율은 약 2.3×10⁻⁵ 치환/뉴클레오티드/복제 주기로, RNA 바이러스 중 높은 편에 속한다. 이는 RNA의존RNA중합효소가 교정(proofreading) 기능이 없기 때문이다. 높은 돌연변이율과 선택압이 결합하여 바이러스의 급속한 항원 변이를 가능하게 한다. 또한 분절형 유전체의 특성상, 서로 다른 바이러스가 동일 세포를 동시 감염할 경우 유전체 분절의 재배열(reassortment)이 발생하여 전혀 새로운 조합의 바이러스가 출현할 수 있다.
5. 항원 변이 기전
항원 소변이는 HA와 NA 유전자의 점돌연변이(point mutation) 축적으로 인해 발생하는 점진적인 항원 변화이다. 면역 선택압 하에서 항체 결합 부위(항원 결정기, epitope)에 변이가 축적되어 기존 면역을 회피할 수 있는 변이주가 선택된다. 이러한 지속적인 항원 소변이로 인해 계절성 인플루엔자 백신 조성을 매년 검토하고 업데이트해야 한다. H3N2 아형이 H1N1보다 항원 소변이 속도가 빠르며, 인플루엔자 B는 A보다 느리다(Petrova & Russell, Nature Reviews Microbiology, 2018).
항원 대변이는 서로 다른 인플루엔자 A 바이러스가 동일한 숙주세포에 동시 감염되었을 때 유전체 분절의 재배열(reassortment)을 통해 발생하는 급격한 항원 변화이다. 새로운 HA 및/또는 NA 아형을 가진 바이러스가 출현하면 인구집단 대부분이 면역학적으로 순진(naive)하여 팬데믹이 발생할 수 있다. 20세기와 21세기의 모든 인플루엔자 팬데믹은 항원 대변이의 결과였다. 인플루엔자 B는 동물 저장숙주가 없어 항원 대변이가 발생하지 않으며, 팬데믹을 일으키지 않는다.
6. 병원성과 임상 양상
인플루엔자의 전형적인 증상은 갑작스러운 발열(38~40°C), 오한, 두통, 근육통, 관절통, 피로감과 함께 마른 기침, 인후통, 비충혈 등의 호흡기 증상이다. 그러나 감염자의 약 50%만이 이러한 전형적 증상을 보이며, 소아에서는 오심, 구토, 설사 등의 소화기 증상이 더 흔하다. 대부분의 건강한 성인에서 증상은 7~10일 내에 자연 회복되나, 기침과 피로감은 수 주간 지속될 수 있다.
잠복기는 평균 약 2일(범위 1~4일)이다. 감염자는 증상 발현 약 1일 전부터 바이러스를 배출하기 시작하며, 증상 발현 후 5~7일간 전염력을 유지한다. 소아와 면역저하자에서는 바이러스 배출 기간이 더 길 수 있다. 전염력은 증상 발현 직후 처음 2~3일간 가장 높다.
중증 합병증으로는 바이러스성 폐렴, 세균성 2차 감염 폐렴(특히 Streptococcus pneumoniae, Staphylococcus aureus), 급성호흡곤란증후군(ARDS), 심근염, 뇌염, 횡문근융해증, 다장기부전 등이 있다. 고위험군에는 65세 이상 고령자, 5세 미만(특히 2세 미만) 소아, 임산부, 만성 폐질환, 심혈관 질환, 당뇨병, 면역저하 환자, 비만자(BMI ≥40) 등이 포함된다.
역전사중합효소연쇄반응(RT-PCR)은 인플루엔자 진단의 표준방법으로, 높은 민감도와 특이도를 가지며 바이러스 유형(A, B) 및 아형(H1, H3, N1, N2 등)의 구분이 가능하다. 다중 RT-PCR은 인플루엔자와 기타 호흡기 바이러스(RSV, SARS-CoV-2 등)를 동시에 검출할 수 있다. 신속 인플루엔자 진단 검사(RIDT)는 15~30분 내에 결과를 제공하며 민감도 50~70%, 특이도 90% 이상이다. 바이러스 배양은 생존 바이러스를 분리하여 상세한 항원 분석 및 약제 감수성 검사에 사용되며, 감시 및 백신 주 선정에 중요하다.
7. 역학과 전파
계절성 인플루엔자는 온대 지역에서 주로 겨울철에 유행하며(북반구 11월~3월, 남반구 5월~9월), 열대 지역에서는 연중 발생한다. WHO는 전 세계적으로 매년 약 10억 건의 감염, 300만~500만 건의 중증 사례, 29만~65만 명의 호흡기 관련 사망이 발생한다고 추정한다(WHO, 2025). 미국에서 2024~2025 시즌은 약 5,100만 건의 인플루엔자 질환, 2,300만 건의 외래 방문, 71만 건의 입원, 4만 5,000명의 사망으로 높은 중증도의 시즌이었다(CDC, 2026).
20세기 이후 주요 인플루엔자 팬데믹은 다음과 같다.
| 팬데믹 | 연도 | 원인 바이러스 | 기원 | 추정 사망자 수 |
|---|---|---|---|---|
| 스페인 독감 | 1918~1919 | A(H1N1) | 미확정 (조류 기원 추정) | 5,000만~1억 명 |
| 아시아 독감 | 1957~1958 | A(H2N2) | 조류-인간 재배열 | 100만~200만 명 |
| 홍콩 독감 | 1968~1969 | A(H3N2) | 조류-인간 재배열 | 100만 명 |
| 러시아 독감 | 1977~1978 | A(H1N1) | 연구실 유출 추정 | 불명 |
| 신종플루 | 2009~2010 | A(H1N1)pdm09 | 돼지-조류-인간 재배열 | 15만~57만 명 |
1918년 스페인 독감은 인류 역사상 가장 치명적인 팬데믹 중 하나로, 전 세계 인구의 약 1/3이 감염되고 5,000만 명 이상이 사망한 것으로 추정된다. 특이하게도 20~40세 건강한 성인에서 높은 사망률을 보였으며, 이는 과도한 면역 반응("사이토카인 폭풍")과 관련이 있는 것으로 추정된다(Taubenberger & Morens, Emerging Infectious Diseases, 2006).
고병원성 조류 인플루엔자 A(H5N1)은 1997년 홍콩에서 처음으로 인간 감염이 확인되었다. WHO의 2025년 12월 19일 기준 누적 데이터에 따르면, 2003년부터 전 세계적으로 993건의 인간 확진 사례가 보고되었으며, 이 중 477명이 사망하여 치명률이 약 48%에 달한다(WHO, 2025년 12월). 지속적인 인간 간 전파는 확인되지 않았으나, 2024년 3월 이후 미국에서 젖소 농장 발생과 관련된 대규모 동물 발생이 확인되었다. 2025년 5월까지 미국 전역 16개 이상의 주에서 약 1,070건의 젖소 농장 발생이 보고되었으며, 71건의 인간 감염이 확인되었다(CDC, 2025). 이후 적극적인 검사와 방역 조치로 발생이 크게 감소하였으나, 야생 조류에서의 광범위한 순환은 지속되고 있다.
8. 면역, 치료, 예방
FDA 승인 인플루엔자 항바이러스제로는 뉴라미니데이스 억제제(oseltamivir, zanamivir, peramivir)와 캡 의존 엔도뉴클레이스 억제제(baloxavir marboxil)가 있다. 오셀타미비르(Tamiflu)는 경구제로 가장 널리 사용되며, 증상 발현 48시간 이내 투여 시 증상 기간을 약 1일 단축하고 합병증 위험을 감소시킨다. 자나미비르(Relenza)는 흡입제, 페라미비르(Rapivab)는 정맥주사제이다. 발록사비르(Xofluza)는 1회 경구 투여로 치료가 완료되는 장점이 있다.
| 약물명 | 상품명 | 기전 | 투여 경로 | 용법 |
|---|---|---|---|---|
| Oseltamivir | Tamiflu | NA 억제제 | 경구 | 75mg 1일 2회, 5일 |
| Zanamivir | Relenza | NA 억제제 | 흡입 | 10mg 1일 2회, 5일 |
| Peramivir | Rapivab | NA 억제제 | 정맥주사 | 600mg 1회 |
| Baloxavir marboxil | Xofluza | 엔도뉴클레이스 억제제 | 경구 | 체중별 1회 투여 |
과거 사용되던 M2 이온 채널 억제제(아만타딘, 리만타딘)는 현재 순환하는 거의 모든 인플루엔자 A 바이러스가 M2에 내성 돌연변이(S31N)를 가지고 있어 더 이상 권장되지 않는다.
계절성 인플루엔자 백신은 가장 효과적인 예방 수단이다. 백신 유형에는 불활성화 백신(IIV), 재조합 백신(RIV), 생약독화 백신(LAIV)이 있다. 2025~2026 시즌부터 모든 인플루엔자 백신은 A(H1N1), A(H3N2), B/Victoria 3개 항원을 포함하는 3가(trivalent) 백신으로 전환되었다(FDA, 2025; CDC, 2026). 백신 효능은 순환 바이러스와의 항원적 일치도에 따라 달라지며, 일반적으로 40~60%의 증상 감염 예방 효과를 보인다. 중증 질환, 입원, 사망 예방 효과는 더 높다.
| 백신 유형 | 약어 | 특징 | 적응 연령 |
|---|---|---|---|
| 불활성화 백신 (표준용량) | IIV-SD | 주사, 가장 흔히 사용 | 6개월 이상 |
| 불활성화 백신 (고용량) | IIV-HD | 65세 이상용, 4배 항원 | 65세 이상 |
| 불활성화 백신 (보강제 첨가) | aIIV | MF59 보강제 포함 | 65세 이상 |
| 재조합 백신 | RIV | 달걀 무사용, 3배 항원 | 18세 이상 |
| 생약독화 백신 | LAIV | 비강 분무 | 2~49세 |
WHO와 각국 보건당국은 65세 이상 고령자, 6개월~5세 소아, 임산부, 만성 질환자, 의료종사자, 요양시설 거주자 및 종사자 등 고위험군에 대해 매년 인플루엔자 백신 접종을 권장한다.
범용 인플루엔자 백신(universal influenza vaccine) 개발이 활발히 진행 중이다. 현재 백신은 HA 머리 부분의 가변 항원을 표적으로 하여 매년 업데이트가 필요하지만, HA 줄기 또는 M2e 등 보존 항원을 표적으로 하는 범용 백신은 광범위하고 지속적인 보호를 제공할 수 있을 것으로 기대된다. 2026년 2월 기준, CIDRAP의 범용 인플루엔자 백신 기술 로드맵에 따르면 다수의 후보 백신이 임상 시험 중이며, mRNA 기반 계절성 인플루엔자 백신(Moderna의 mRNA-1010 등)도 3상 임상 시험 결과가 보고되고 있다(CIDRAP, 2026). WHO는 2025년 12월 차세대 인플루엔자 백신에 대한 업데이트된 선호 제품 특성(Preferred Product Characteristics)을 발표하였다(WHO, 2026).
손 위생, 기침 에티켓, 마스크 착용, 아픈 사람과의 접촉 회피, 환기 등이 전파 감소에 효과적이다. 유행 시기에 의심 증상이 있는 환자는 해열 후 24시간이 경과할 때까지 자가격리가 권장된다.
9. 자연 숙주 및 동물 감염
야생 수금류(오리, 거위, 백조 등)는 인플루엔자 A 바이러스의 주요 자연 저장숙주로, 거의 모든 HA(18종)와 NA(11종) 아형이 이들에서 발견된다. 대부분의 조류 인플루엔자 바이러스는 야생 조류에서 무증상 장 감염을 일으키며, 분변-구강 경로로 전파된다. 철새의 이동은 바이러스의 광역 전파에 중요한 역할을 한다.
닭, 칠면조 등의 가금류는 조류 인플루엔자에 감수성이 높다. 저병원성 조류 인플루엔자(LPAI)는 경증 증상을 유발하지만, 고병원성 조류 인플루엔자(HPAI, 특히 H5 및 H7 아형 일부)는 가금류에서 치명률이 100%에 달하는 급성 전신 감염을 일으켜 막대한 경제적 피해를 초래한다.
돼지는 인플루엔자 A 바이러스의 중요한 숙주로, 돼지에서 순환하는 주요 아형은 H1N1, H1N2, H3N2이다. 돼지는 α2,3- 및 α2,6-연결 시알산 수용체를 모두 발현하여 조류 및 인간 바이러스의 동시 감염이 가능하며, 이는 재배열에 의한 새로운 바이러스 출현의 중요한 경로이다. 2009년 H1N1 팬데믹 바이러스는 돼지, 조류, 인간 인플루엔자 바이러스 유전자 분절이 복합적으로 재배열된 결과였다(Neumann et al., Nature, 2009).
말(H3N8, H7N7), 개(H3N8, H3N2), 고양이, 해양 포유류(물개, 고래) 등에서도 인플루엔자 A 바이러스 감염이 보고된다. 2024년 3월 이후 미국에서 젖소 농장에서의 H5N1 발생이 처음 확인되어, 소가 새로운 중간숙주로 부상할 가능성에 대한 우려가 제기되었다. 이 발생은 B3.13 유전형에 의한 것이었으며, 2025년 초에는 새로운 D1.1 유전형이 젖소에서 확인되었다(USDA, 2025). 이후 적극적 방역으로 발생이 크게 감소하였으나, 이 사례는 인플루엔자 바이러스의 예측 불가능한 숙주 확장 능력을 보여주는 중요한 사례로 기록되고 있다.
10. 연구사와 과학적 의의
인플루엔자 바이러스 연구는 현대 바이러스학의 발전에 핵심적인 기여를 해왔다. 1931년 리처드 쇼프(Richard Shope)가 돼지에서 인플루엔자 바이러스를 분리한 것이 동물 인플루엔자 연구의 시작이었으며, 1933년 윌슨 스미스, 크리스토퍼 앤드류스, 패트릭 레이들로가 인간에서 최초로 인플루엔자 바이러스를 분리하였다(Smith et al., The Lancet, 1933). 1940년대 토머스 프랜시스(Thomas Francis Jr.)와 조너스 솔크(Jonas Salk)가 불활성화 인플루엔자 백신을 개발하였으며, 이후 인플루엔자 백신은 지속적으로 개선되어 왔다.
2005년 제프리 타우벤버거(Jeffery Taubenberger) 연구팀이 영구동토층에 보존된 1918년 스페인 독감 희생자의 조직에서 바이러스 유전체를 완전히 재구성하는 데 성공하였으며, 이를 통해 바이러스의 높은 병원성에 기여한 유전적 특성이 규명되었다. 역유전학(reverse genetics) 기술의 발전은 인플루엔자 바이러스 연구와 백신 개발에 혁명적 변화를 가져왔다.
현재 연구의 주요 방향으로는 범용 인플루엔자 백신 개발, mRNA 플랫폼 기반 인플루엔자 백신 개발, 조류 인플루엔자의 종간 전파 메커니즘 규명, 인플루엔자 감염 후 장기 후유증("롱플루") 연구, 항바이러스제 내성 감시, 그리고 인플루엔자의 계절성 유행 기전 규명 등이 있다.
11. 근연 바이러스 비교
| 특성 | 인플루엔자 A | 인플루엔자 B | 인플루엔자 C | 인플루엔자 D |
|---|---|---|---|---|
| 유전체 분절 수 | 8 | 8 | 7 | 7 |
| 숙주 범위 | 인간, 조류, 돼지, 말 등 | 인간 (해양 포유류 드묾) | 인간, 돼지 | 소, 돼지 |
| 아형/계통 분류 | HA, NA 아형 | 계통 (Victoria, Yamagata) | 해당 없음 | 해당 없음 |
| 항원 대변이 | 발생함 | 발생하지 않음 | 발생하지 않음 | 발생하지 않음 |
| 팬데믹 잠재력 | 높음 | 없음 | 없음 | 없음 |
| 질병 중증도 | 중등도~중증 | 경증~중등도 | 경증 | 인간 질병 미확인 |
| 계절성 유행 | 주요 원인 | 주요 원인 | 드묾 | 해당 없음 |
| 백신 포함 | 포함 | 포함 | 미포함 | 미포함 |
인플루엔자 A 바이러스는 넓은 숙주 범위와 항원 대변이 능력으로 인해 팬데믹 잠재력이 가장 높으며, 지속적인 감시의 핵심 대상이다. 인플루엔자 B는 인간 중심 순환에 한정되지만 특히 소아와 고령자에서 상당한 질병 부담을 유발한다.
12. 미해결 질문
첫째, 범용 인플루엔자 백신의 실용화 시점과 효능은 여전히 불확실하다. HA 줄기, M2e, 뉴라미니데이스 등 보존 항원을 표적으로 하는 다양한 접근법이 임상 시험 중이나, 광범위하고 지속적인 보호 효과를 입증하기까지 추가 연구가 필요하다.
둘째, H5N1 및 기타 조류 인플루엔자 바이러스가 인간 간 효율적 전파 능력을 획득할 수 있는 유전적 변화의 정확한 요건은 아직 완전히 규명되지 않았다. 2024~2025년 미국 젖소 발생은 바이러스의 포유류 적응 과정에 대한 새로운 데이터를 제공하였으나, 팬데믹 위험 평가에는 여전히 불확실성이 존재한다.
셋째, 인플루엔자 바이러스가 계절성 유행 패턴을 보이는 정확한 기전은 여전히 논쟁 중이다. 온도, 습도, 자외선, 인간 행동 패턴, 면역 상태 등 복합적 요인이 관여하는 것으로 추정된다.
넷째, 항바이러스제 내성의 출현과 확산을 모니터링하고 대응하는 것이 지속적 과제이다. 발록사비르의 경우 치료 중 내성 변이 출현이 보고되어 주의가 필요하다.
다섯째, 인플루엔자 감염 후 장기 후유증("롱플루")에 대한 연구가 초기 단계에 있으며, COVID-19의 롱코비드와 유사한 피로, 인지기능 저하 등의 장기 증상이 보고되고 있으나 그 빈도와 기전은 아직 불명확하다.
13. 참고문헌
Smith, W., Andrewes, C.H., & Laidlaw, P.P. (1933). A virus obtained from influenza patients. The Lancet, 222(5732), 66-68. https://doi.org/10.1016/S0140-6736(00)78541-2
Webster, R.G., Bean, W.J., Gorman, O.T., et al. (1992). Evolution and ecology of influenza A viruses. Microbiological Reviews, 56(1), 152-179. https://doi.org/10.1128/mr.56.1.152-179.1992
Taubenberger, J.K., & Morens, D.M. (2006). 1918 Influenza: the mother of all pandemics. Emerging Infectious Diseases, 12(1), 15-22. https://doi.org/10.3201/eid1201.050979
Neumann, G., Noda, T., & Kawaoka, Y. (2009). Emergence and pandemic potential of swine-origin H1N1 influenza virus. Nature, 459(7249), 931-939. https://doi.org/10.1038/nature08157
Gamblin, S.J., & Skehel, J.J. (2010). Influenza hemagglutinin and neuraminidase membrane glycoproteins. Journal of Biological Chemistry, 285(37), 28403-28409. https://doi.org/10.1074/jbc.R110.129809
Krammer, F., Smith, G.J.D., Fouchier, R.A.M., et al. (2018). Influenza. Nature Reviews Disease Primers, 4, 3. https://doi.org/10.1038/s41572-018-0002-y
Petrova, V.N., & Russell, C.A. (2018). The evolution of seasonal influenza viruses. Nature Reviews Microbiology, 16(1), 47-60. https://doi.org/10.1038/nrmicro.2017.118
Long, J.S., Mistry, B., Haslam, S.M., & Barclay, W.S. (2019). Host and viral determinants of influenza A virus species specificity. Nature Reviews Microbiology, 17(2), 67-81. https://doi.org/10.1038/s41579-018-0115-z
Morens, D.M., Taubenberger, J.K., & Fauci, A.S. (2009). The persistent legacy of the 1918 influenza virus. New England Journal of Medicine, 361(3), 225-229. https://doi.org/10.1056/NEJMp0904819
Caini, S., Meijer, A., Nunes, M.C., et al. (2024). Probable extinction of influenza B/Yamagata and its public health implications. The Lancet Microbe, 5(7), e614-e622. https://doi.org/10.1016/S2666-5247(24)00066-1
World Health Organization (WHO). (2025). Influenza (Seasonal). https://www.who.int/news-room/fact-sheets/detail/influenza-(seasonal)
World Health Organization (WHO). (2025). Cumulative number of confirmed human cases for avian influenza A(H5N1) reported to WHO, 2003-2025, 19 December 2025. https://www.who.int/publications/m/item/cumulative-number-of-confirmed-human-cases-for-avian-influenza-a(h5n1)-reported-to-who--2003-2025--19-december-2025
Centers for Disease Control and Prevention (CDC). (2026). 2024-2025 Influenza Season Summary. https://www.cdc.gov/flu-burden/php/data-vis-vac/2024-2025-prevented.html
Centers for Disease Control and Prevention (CDC). (2026). 2025-2026 Flu Season. https://www.cdc.gov/flu/season/2025-2026.html
U.S. Food and Drug Administration (FDA). (2025). Influenza Vaccine Composition for the 2025-2026 U.S. Influenza Season. https://www.fda.gov/vaccines-blood-biologics/influenza-vaccine-composition-2025-2026-us-influenza-season
NCBI Insights. (2023). Upcoming changes to influenza virus names in NCBI Taxonomy. https://ncbiinsights.ncbi.nlm.nih.gov/2023/02/21/influenza-virus-ncbi-taxonomy/
Plotkin, S.A., Orenstein, W.A., Offit, P.A., & Edwards, K.M. (2018). Plotkin's Vaccines (7th ed.). Elsevier.
Yoon, S.W., Webby, R.J., & Webster, R.G. (2014). Evolution and ecology of influenza A viruses. Current Topics in Microbiology and Immunology, 385, 359-375. https://doi.org/10.1007/82_2014_396
Bouvier, N.M., & Palese, P. (2008). The biology of influenza viruses. Vaccine, 26(Suppl 4), D49-D53. https://doi.org/10.1016/j.vaccine.2008.07.039
CIDRAP. (2026). Universal Influenza Vaccine Technology Landscape. https://ivr.cidrap.umn.edu/
재미있는 사실
인플루엔자 바이러스는 RNA 바이러스 중에서 핵 내에서 복제하는 드문 바이러스 중 하나입니다. 대부분의 RNA 바이러스는 세포질에서 복제하지만, 인플루엔자는 핵 내에서 전사와 복제가 이루어지며, 이는 숙주 세포의 스플라이싱 기구를 이용하여 M 및 NS 유전자에서 두 개의 다른 단백질을 만들기 위함입니다.
야생 오리와 거위는 인플루엔자 A 바이러스의 자연 저장숙주로, 거의 모든 알려진 HA(18종)와 NA(11종) 아형의 조합이 이들에서 발견됩니다. 놀랍게도 야생 수금류에서 인플루엔자 바이러스는 주로 장에서 복제되며 무증상 감염을 일으키고, 분변을 통해 환경으로 방출되어 물을 통해 다른 조류로 전파됩니다.
1918년 스페인 독감의 원인 바이러스 유전체는 영구동토층에 보존된 희생자의 조직과 포르말린 고정 조직 표본에서 회수되어 2005년에 완전히 재구성되었습니다. 이 연구를 통해 바이러스의 높은 병원성에 기여한 유전적 특성이 규명되었으며, 조류 기원 바이러스가 직접 인간에 적응했을 가능성이 제시되었습니다.
돼지는 α2,3- 및 α2,6-연결 시알산 수용체를 모두 발현하여 조류와 인간 인플루엔자 바이러스가 동시에 감염될 수 있는 "혼합 용기(mixing vessel)" 역할을 합니다. 이러한 동시 감염은 유전체 분절의 재배열을 통해 새로운 팬데믹 바이러스의 출현으로 이어질 수 있으며, 2009년 H1N1 팬데믹 바이러스가 그 대표적 예입니다.
인플루엔자 바이러스의 뉴라미니데이스(NA)는 숙주세포 표면과 점액의 시알산을 절단하여 새로 형성된 바이러스의 방출을 돕습니다. 오셀타미비르(타미플루)와 자나미비르(렐렌자) 같은 항바이러스제는 NA를 억제하여 바이러스 방출을 차단함으로써 감염 확산을 제한합니다.
인플루엔자 바이러스의 M2 단백질은 양성자 이온 채널 기능을 가지며, 과거 아만타딘과 리만타딘 같은 항바이러스제의 표적이었습니다. 그러나 현재 순환하는 거의 모든 인플루엔자 A 바이러스가 M2에 내성 돌연변이(S31N)를 가지고 있어 이 약물들은 더 이상 권장되지 않습니다.
계절성 인플루엔자 백신 조성은 WHO의 글로벌 인플루엔자 감시대응체계(GISRS)를 통해 결정됩니다. 전 세계 143개국 이상의 국가인플루엔자센터에서 수집된 바이러스 표본이 6개 WHO 협력센터에서 분석되어, 매년 2월(북반구)과 9월(남반구)에 다음 계절 백신 조성이 권고됩니다.
인플루엔자 바이러스는 다형성(pleomorphic) 형태를 가지며, 실험실 적응 주는 주로 구형(직경 약 100nm)이지만 임상 분리주는 길이가 수 μm에 달하는 사상형(filamentous)이 더 흔합니다. 흥미롭게도 바이러스 형태는 숙주세포 유형과 M1 단백질의 특정 아미노산 잔기에 의해 결정됩니다.
2009년 H1N1 팬데믹 바이러스(A(H1N1)pdm09)는 복잡한 재배열의 산물입니다. 이 바이러스는 북미 돼지 인플루엔자(트리플 재배열 바이러스), 유라시아 조류 유래 돼지 인플루엔자, 그리고 인간 H3N2 바이러스에서 유래한 유전자 분절을 조합하고 있습니다.
B/Yamagata 계통 인플루엔자 바이러스는 COVID-19 팬데믹 기간의 비약물적 중재 조치로 인해 2020년 3월 이후 전 세계적으로 검출되지 않고 있으며, 사실상 소멸한 것으로 판단됩니다. 이에 따라 2025~2026 시즌부터 모든 인플루엔자 백신은 B/Victoria만 포함하는 3가 백신으로 전환되었습니다.
2024년 3월, 미국에서 사상 최초로 젖소에서 고병원성 조류 인플루엔자 H5N1 감염이 확인되었습니다. 이전까지 소는 인플루엔자의 주요 숙주로 간주되지 않았으나, 이 발생은 인플루엔자 바이러스의 예측 불가능한 숙주 범위 확장 능력을 보여주는 중요한 사례가 되었습니다.
인플루엔자 바이러스는 'cap-snatching'이라는 독특한 전략으로 mRNA를 합성합니다. 바이러스 중합효소가 숙주 세포의 pre-mRNA에서 5' 캡 구조를 포함한 짧은 서열(10~13개 뉴클레오티드)을 절단하여 자신의 mRNA 합성을 위한 프라이머로 사용하는 것입니다.
FAQ
인플루엔자와 감기(common cold)는 모두 호흡기 바이러스 감염이지만 원인 바이러스와 증상 중증도가 다릅니다. 인플루엔자는 인플루엔자 바이러스가 원인이고, 갑작스러운 고열(38~40°C), 심한 근육통, 두통, 극심한 피로감이 특징입니다. 감기는 주로 리노바이러스, 코로나바이러스(계절성) 등이 원인이며, 콧물, 코막힘, 재채기, 경미한 인후통이 주 증상이고 발열은 드물거나 경미합니다. 인플루엔자는 폐렴 등 심각한 합병증을 유발할 수 있어 백신과 항바이러스제가 있지만, 감기에는 특이적 치료제가 없습니다.
인플루엔자 백신은 증상 감염을 완전히 예방하지는 못합니다. 백신 효능은 순환 바이러스와 백신 주의 항원적 일치도에 따라 달라지며, 일반적으로 40~60%의 증상 감염 예방 효과를 보입니다. 그러나 백신을 맞으면 감염되더라도 증상이 경미해지고, 폐렴 등 중증 합병증, 입원, 사망 위험이 크게 감소합니다. 특히 고령자, 만성 질환자, 어린이 등 고위험군에서 백신의 이점이 큽니다. 또한 불활성화 백신은 죽은 바이러스를 사용하므로 백신 자체가 독감을 유발하지 않습니다.
인플루엔자 바이러스는 항원 소변이(antigenic drift)를 통해 지속적으로 변화하기 때문입니다. HA와 NA 표면 단백질의 점돌연변이가 축적되어 기존 면역을 회피하는 새로운 변이주가 출현합니다. 이에 따라 WHO는 매년 2월(북반구)과 9월(남반구)에 다음 계절 백신 조성을 권고하며, 순환 가능성이 높은 바이러스 주를 선정합니다. 또한 백신에 의한 면역도 시간이 지나면 감소하므로, 매년 접종이 최적의 보호를 위해 권장됩니다.
H5N1을 포함한 조류 인플루엔자 바이러스는 인간에게 감염될 수 있지만, 현재까지 지속적인 인간 간 전파는 확인되지 않았습니다. 인간 감염은 주로 감염된 가금류나 오염된 환경, 또는 감염 젖소에 직접 노출될 때 발생합니다. WHO의 2025년 12월 기준 누적 데이터에 따르면, 2003년 이후 전 세계적으로 993건의 H5N1 인간 확진 사례와 477명의 사망이 보고되어 치명률이 약 48%에 달합니다. 바이러스가 인간 간 효율적 전파 능력을 획득할 경우 심각한 팬데믹이 우려되어, 전 세계적으로 지속적인 감시와 팬데믹 대비가 이루어지고 있습니다.
오셀타미비르(타미플루)를 포함한 인플루엔자 항바이러스제는 증상 발현 후 48시간 이내에 투여할 때 가장 효과적입니다. 조기 투여 시 증상 기간을 약 1일 단축하고, 합병증 위험을 감소시킵니다. 그러나 48시간이 지났더라도 중증 환자나 입원 환자, 고위험군에서는 투여가 권장됩니다. 모든 인플루엔자 환자에게 항바이러스제가 필요한 것은 아니며, 건강한 성인의 경증 감염은 대부분 대증요법으로 자연 회복됩니다. 고위험군, 중증 환자, 입원 환자에서 항바이러스제 투여가 특히 권장됩니다.
인플루엔자 A형과 B형은 증상은 유사하지만 여러 중요한 차이가 있습니다. A형은 인간, 조류, 돼지, 말 등 다양한 숙주에 감염되고 HA/NA 아형으로 분류되며, 항원 대변이를 통해 팬데믹을 일으킬 수 있습니다. B형은 주로 인간만 감염시키고 Victoria/Yamagata 계통으로 분류되며, 항원 대변이가 없어 팬데믹을 일으키지 않습니다. 일반적으로 A형이 더 중증 질환을 유발하는 경향이 있으나, B형도 특히 어린이와 고령자에서 심각한 질환을 일으킬 수 있습니다. 두 유형 모두 계절성 인플루엔자 백신에 포함됩니다.
인플루엔자 감염자는 증상 발현 약 1일 전부터 바이러스를 배출하기 시작하며, 증상 발현 후 5~7일간 전염력을 유지합니다. 전염력은 증상 발현 직후 처음 2~3일간 가장 높습니다. 어린이와 면역저하자에서는 바이러스 배출 기간이 10일 이상으로 더 길 수 있습니다. 따라서 증상이 있는 환자는 해열 후 24시간이 경과할 때까지 자가격리하고, 다른 사람과의 접촉을 피하는 것이 권장됩니다.
1918년 스페인 독감은 여러 요인이 복합적으로 작용하여 치명적이었습니다. 첫째, H1N1 바이러스가 완전히 새로운 항원을 가져 인구 대부분이 면역학적으로 순진했습니다. 둘째, 바이러스의 특정 유전적 특성이 과도한 면역 반응("사이토카인 폭풍")을 유발하여 건강한 젊은 성인에서 높은 사망률을 초래했습니다. 셋째, 당시에는 항생제가 없어 세균성 2차 폐렴을 치료할 수 없었습니다. 넷째, 제1차 세계대전으로 인한 군대 이동과 과밀 환경이 전파를 촉진했습니다. 전 세계 인구의 약 1/3이 감염되고 5,000만~1억 명이 사망한 것으로 추정되어, 인류 역사상 가장 치명적인 팬데믹 중 하나로 기록됩니다.
B/Yamagata 계통 인플루엔자 바이러스는 2020년 3월 이후 전 세계 감시 시스템에서 검출되지 않고 있으며, 사실상 소멸(probable extinction)한 것으로 판단됩니다. COVID-19 팬데믹 기간의 비약물적 중재 조치(마스크, 사회적 거리두기, 여행 제한)가 주요 원인으로, 같은 시기 B/Victoria 계통은 조치 완화 후 재유행하였지만 B/Yamagata는 복귀하지 못했습니다. 2024년 Lancet Microbe에 발표된 체계적 문헌 고찰에서도 이를 확인하였으며, 이에 따라 2025~2026 시즌부터 모든 인플루엔자 백신에서 B/Yamagata 항원이 제외되었습니다.
CDC의 추산에 따르면 2024~2025 미국 인플루엔자 시즌은 높은 중증도의 시즌이었습니다. 약 5,100만 건의 인플루엔자 질환, 2,300만 건의 외래 방문, 71만 건의 입원, 4만 5,000명의 사망이 발생한 것으로 추정되며, 이는 2010~2011 시즌 이후 가장 높은 입원율을 기록한 것입니다. 75세 이상 고령자에서 입원 부담이 가장 높았으며, 입원 환자의 10만 명당 약 599명이 75세 이상이었습니다.
갤러리
4 장의 이미지 인플루엔자 바이러스
인플루엔자 바이러스인플루엔자 바이러스
 인플루엔자 바이러스
인플루엔자 바이러스인플루엔자 바이러스
 인플루엔자 바이러스
인플루엔자 바이러스인플루엔자 바이러스
 인플루엔자 바이러스
인플루엔자 바이러스인플루엔자 바이러스