메탄생성균
고세균 · other
Methanogenic archaea
학명 유래: "메탄을 생성하는(methane-generating) 고세균. 그리스어 methane(메탄)과 -genes(~을 생성하는)의 조합."
발견
미생물 특성
서식지
분류 변천사
1936년 Kluyver & van Niel이 Methanobacterium, Methanosarcina 속을 명명. 1977년 Woese & Fox의 16S rRNA 분석으로 세균과 구별되는 고세균(Archaea) 영역에 속함이 밝혀짐. 전통적으로 Euryarchaeota 문에 배치되었으나, GTDB 분류 체계에서는 Methanobacteriota, Halobacteriota, Thermoplasmatota 등 여러 문으로 재분류됨. 메타게노믹스를 통해 Thermoproteota, Asgardarchaeota 등에서도 MCR 유전자 보유 계통 발견.
임상적 의미
직접적 병원성 없음. 인간 장내 공생체(*Methanobrevibacter smithii*)로서 소화 효율에 관여하며, 과도한 메탄 생성 시 변비·팽만감 등 소화기 증상과 연관 가능성 보고.

메탄생성균(Methanogenic archaea, 또는 Methanogens)은 메탄(CH₄)을 대사의 최종 산물로 생성하는 고세균(Archaea)의 다계통 집단이다. 생명의 3역(Domain) 중 고세균역에 속하며, 산소가 없는 환경에서 절대 혐기성 대사를 수행한다. 메탄 생성(Methanogenesis)은 이들이 ATP를 생산하는 유일한 생화학적 경로로, 수소와 이산화탄소, 아세트산, 메탄올, 메틸아민 등의 기질을 사용하여 메탄을 만들어낸다. 모든 메탄생성균은 메틸-조효소 M 환원효소(Methyl-coenzyme M reductase, MCR)라는 독특한 효소 시스템을 보유하며, 이 효소는 메탄 분자를 직접 형성하는 최종 반응을 촉매한다.
메탄생성균은 지구상에서 생물학적 메탄을 생산하는 유일한 생물군으로서, 전 세계 메탄 배출량의 약 60~70%를 차지한다. 이들은 습지, 해저 퇴적물, 반추동물의 소화관, 흰개미 후장, 인간 장내, 하수처리장, 논토양, 매립지, 심해 열수분출공 등 다양한 혐기성 환경에 서식한다. 현재까지 약 150종 이상이 배양·기재되었으며(DSMZ 기준), 최소 3개 문(Phylum), 7개 이상의 목(Order)에 분포하는 다계통군(polyphyletic group)이다. 유전체 크기는 약 1.24 Mb(Methanothermus fervidus)에서 약 5.75 Mb(Methanosarcina acetivorans)까지 종에 따라 크게 다르다.
메탄생성균은 지구 초기 역사(약 35억 년 전)부터 존재했을 것으로 추정되는 가장 오래된 생물군 중 하나이며, 지구 탄소 순환과 기후 시스템에 핵심적인 역할을 한다. 메탄은 100년 기준 지구온난화 지수(GWP)가 약 28~34로 이산화탄소보다 훨씬 강력한 온실가스이므로, 메탄생성균의 활동은 기후 변화와 직결된다. 한편 이들의 대사를 활용한 바이오가스 생산 기술은 재생 에너지원으로서 산업적 가치가 크다. 1936년 네덜란드의 A. J. Kluyver와 C. B. van Niel이 메탄생성 미생물을 독립적인 분류군(Methanobacterium, Methanosarcina 등)으로 처음 명명하였으며, 같은 해 H. A. Barker가 Methanobacterium omelianskii를 최초로 순수 배양(후일 혼합 배양으로 판명)하여 메탄생성균 연구의 시대를 열었다.
1. 개요
메탄생성균이라는 이름은 '메탄을 생성하는(methane-generating)'이라는 의미에서 유래했다. 그리스어 methane(메탄)과 -genes(~을 생성하는)의 조합이며, 이들이 에너지 대사의 부산물로 메탄 가스를 필수적으로 생성하는 특성을 직접 반영한다.
분류학적으로 메탄생성균은 단일 계통군(monophyletic group)이 아니라 다계통군(polyphyletic group)이다. 즉, 공통 조상에서 유래한 하나의 분류군이 아니라 메탄 생성이라는 대사적 특성을 공유하는 여러 독립 계통을 묶은 기능적 그룹이다. 전통적으로 Euryarchaeota 문에 속하는 것으로 알려졌으나, GTDB(Genome Taxonomy Database) 분류 체계에서는 Methanobacteriota, Halobacteriota, Thermoplasmatota 등 여러 문에 걸쳐 분포하는 것으로 재분류되었다. 최근 메타게노믹스 연구를 통해 Thermoproteota(구 TACK superphylum)와 Asgardarchaeota에서도 MCR 유전자를 보유한 계통이 발견되어, 메탄 생성 능력의 분포가 예상보다 훨씬 넓다는 사실이 밝혀지고 있다.
메탄생성균의 가장 중요한 공통 특성은 절대 혐기성(strictly anaerobic)이라는 점이다. 산소에 노출되면 MCR의 보조인자인 F₄₃₀를 비롯한 핵심 효소들이 비가역적으로 손상되어 수분 내에 사멸한다. 이 때문에 배양과 연구에 특수한 혐기 기술이 요구된다.
2. 분류와 계통
메탄생성균은 고세균역(Domain Archaea)에 속하며, 현재 배양된 모든 종은 전통 분류 체계에서 Euryarchaeota 문에 포함된다. 그러나 GTDB 분류 체계(release 95 이후)에서는 이들이 Methanobacteriota(구 Euryarchaeota의 일부)와 Halobacteriota로 나뉘며, 일부 메틸영양형 메탄생성균은 Thermoplasmatota에 배치된다. 이러한 분류학적 재배치는 전체 유전체 기반 계통분석의 발전에 따른 것이다.
전통 분류 체계에서 메탄생성균은 5~7개의 목(Order)으로 나뉜다. Methanobacteriales는 막대형 세포를 가진 수소영양형 메탄생성균으로, Methanobacterium, Methanobrevibacter, Methanothermobacter 등이 포함되며, 인간 장내에서 가장 우세한 Methanobrevibacter smithii가 이 목에 속한다. Methanococcales는 구형 세포의 해양성 메탄생성균으로, 열수분출공에서 흔히 발견된다. Methanomicrobiales는 다양한 세포 형태를 보이며, 담수와 해양 퇴적물에 분포한다. Methanosarcinales는 대사적으로 가장 다재다능한 그룹으로, 수소, 아세트산, 메틸화 화합물 등 다양한 기질을 이용할 수 있으며 Methanosarcina와 Methanosaeta(현재 Methanotrix로 재명명)가 대표속이다. Methanopyrales는 초고온성 메탄생성균으로, 122°C에서도 증식 가능한 Methanopyrus kandleri가 유일한 속이다.
비교적 최근에 인정된 목으로 Methanocellales(논토양에서 처음 발견)와 Methanomassiliicoccales(동물 장내에서 발견, 메틸화 화합물과 수소를 동시에 이용)가 있다. Methanomassiliicoccales는 Thermoplasmatota 문에 속하며, 전통적인 Euryarchaeota 메탄생성균과는 계통적으로 상당히 거리가 있다.
메탄생성의 진화적 기원에 대해서는 활발한 논쟁이 계속되고 있다. 2023년 PNAS Nexus에 발표된 연구(Adam et al.)는 메탄(및 기타 알칸) 대사가 고세균의 기원 이전에 이미 존재했을 가능성을 제시하였다. 일부 연구자들은 마지막 고세균 공통 조상(LACA)이 메탄생성균이었을 가능성을 지지하지만, 다른 연구자들은 메탄생성이 고세균 내에서 여러 차례 독립적으로 수평 유전자 전이(HGT)를 통해 전파되었다는 견해를 제시한다. 특히 MCR 유전자 클러스터(mcrABCDG)가 여러 계통에서 발견되는 패턴은 수직적 유전과 수평적 전이의 복합 작용으로 설명되고 있다.
| 분류 단계 | 전통 분류 | GTDB 분류 |
|---|---|---|
| 역(Domain) | Archaea | Archaea |
| 문(Phylum) | Euryarchaeota | Methanobacteriota, Halobacteriota, Thermoplasmatota |
| 대표 강(Class) | Methanobacteria, Methanococci, Methanopyri, Methanomicrobia | Methanobacteria, Methanococci, Methanopyri, Methanocellia 등 |
| 대표 목(Order) | Methanobacteriales, Methanococcales, Methanomicrobiales, Methanosarcinales, Methanopyrales, Methanocellales, Methanomassiliicoccales | (동일) |
3. 형태와 구조
메탄생성균은 형태적으로 매우 다양하다. 구형(coccoid) 세포는 Methanococcus, Methanothermococcus 등에서 관찰되며, 직경 약 0.5~2 μm이다. 막대형(rod-shaped) 세포는 Methanobacterium, Methanothermobacter 등에서 발견되며, 길이 약 2~10 μm, 너비 약 0.4~1 μm이다. Methanospirillum hungatei는 나선형(spiral) 세포로 길이 약 7 μm에 달한다. Methanosarcina는 불규칙한 구형 세포가 덩어리(aggregate)를 형성하며, 개별 세포는 직경 약 1~3 μm이지만 덩어리는 수십 μm에 이를 수 있다. Methanoplanus 등에서는 판형(plate-shaped) 세포가 관찰된다.
세포벽 구조는 세균의 펩티도글리칸과 근본적으로 다르다. Methanobacteriales와 Methanopyrales는 슈도펩티도글리칸(pseudopeptidoglycan)을 가지는데, 이는 세균의 펩티도글리칸과 형태적으로 유사하지만 N-아세틸타로사미누론산(N-acetyltalosaminuronic acid)과 β(1→3) 글리코사이드 결합을 포함하여 화학적으로 구별된다. 대부분의 메탄생성균은 세포 표면에 단백질로 구성된 S-층(S-layer)을 가지며, 이는 격자 형태의 결정 구조를 형성한다. Methanosarcina의 일부 종은 메타노콘드로이틴(methanochondroitin)이라는 독특한 세포외 다당류층을 가진다.
세포막은 고세균 특유의 이소프레노이드 에테르 지질로 구성된다. 세균이나 진핵생물의 에스테르 결합 지질과 대비되는 이 에테르 결합(-O-) 구조는 극한 환경에서의 막 안정성에 기여한다. 일부 고온성 종에서는 세포막을 관통하는 테트라에테르 지질이 발견되어 열안정성을 더욱 높인다.
일부 메탄생성균은 아르카엘럼(archaellum)이라 불리는 운동 기관을 보유한다. 이는 세균의 편모(flagellum)와 기능적으로 유사하지만 구조와 조립 메커니즘이 근본적으로 다르며, 필라멘트 직경이 약 10~13 nm로 세균 편모(약 20 nm)보다 가늘다. 일부 종은 부력 조절을 위한 기체 소낭(gas vesicles)을 가진다.
메탄생성균의 가장 특징적인 시각적 표지는 F₄₂₀ 자가형광이다. 조효소 F₄₂₀의 존재로 인해 420 nm 파장의 자외선을 조사하면 청록색(약 470 nm) 형광을 발한다. 이 특성은 복잡한 미생물 군집에서 메탄생성균을 형광현미경으로 식별하고 정량하는 데 활용된다.
4. 유전체와 분자생물학
메탄생성균의 유전체는 원형 이중가닥 DNA(circular dsDNA)로 구성되며, 크기는 종에 따라 매우 다양하다. 2023년 Microbial Genomics에 발표된 메탄생성균 핵심 유전체(core genome) 및 범유전체(pangenome) 분석 연구(Prondzinsky et al.)에 따르면, 배양된 메탄생성균의 유전체 크기는 약 1.24 Mb(Methanothermus fervidus)에서 약 5.75 Mb(Methanosarcina acetivorans)까지 분포한다. GC 함량은 약 27~62%로 매우 넓은 범위를 보이며, 대부분 1,500~3,500개의 단백질 코딩 유전자를 가진다. 고온성(thermotolerant) 메탄생성균은 저온 적응형(psychrotolerant)에 비해 평균 약 30% 작은 유전체를 가지는 경향이 있으며, 이는 온도가 계통보다 유전체 크기에 더 큰 영향을 미침을 시사한다.
86종의 배양된 메탄생성균에 대한 비교 유전체 분석에서, 확장된 핵심 유전체(extended core genome)는 552개의 오르토그룹(orthogroup)으로 구성되어 전체 유전체의 약 33.7%를 차지한다. 이 핵심 유전체의 대부분(57%)은 생합성 관련 유전자이며, 조효소 수송 및 대사(13%)가 그 뒤를 잇는다. 이처럼 3개 문에 걸친 다계통 생물군임에도 큰 핵심 유전체를 공유한다는 사실은, 메탄생성이라는 공유 생화학이 유전체 구성에 강한 제약을 가한다는 것을 보여준다.
메탄생성에 필수적인 핵심 유전자 클러스터는 다음과 같다. mcrABCDG는 메틸-조효소 M 환원효소(MCR)를 코딩하며, 메탄생성의 최종 단계를 촉매한다. fmdABC/fwdABC는 포르밀메타노푸란 탈수소효소를 코딩하여 CO₂ 환원의 첫 단계를 담당한다. mtrA-H는 메틸-H₄MPT:CoM 메틸전이효소를 코딩하여 에너지 보존에 핵심적인 나트륨 이온 펌핑을 수행한다. 이들 유전자는 모든 메탄생성균에 보존되어 있으며, 특히 mcrA 유전자는 메탄생성균 검출과 다양성 분석의 분자 마커로 널리 사용된다.
고온 적응과 관련하여, 고온성 메탄생성균은 역전사효소(reverse gyrase)와 금속 수송체 유전자를 특이적으로 보유하는 반면, 저온 적응형은 세포막 및 세포벽 관련 유전자, 샤페론 유전자가 풍부하다. 흥미롭게도 아미노산 조성 분석에서 고온성 종은 하전 아미노산(리신, 글루탐산)과 소수성 아미노산(루신, 이소루신)이 증가하며, 저온 적응형은 극성 비하전 아미노산(글루타민, 트레오닌)이 증가하는 경향을 보인다.
수평 유전자 전이(HGT)는 메탄생성균의 진화에서 중요한 역할을 했다. 메탄생성 관련 유전자 클러스터가 여러 계통에서 독립적으로 전이된 증거가 보고되어 있으며, 이는 메탄생성균이 다계통적으로 분포하게 된 원인 중 하나로 제안된다.
5. 생화학과 대사
메탄생성은 세 가지 주요 경로로 구분된다. 수소영양형(hydrogenotrophic) 경로는 가장 보편적이며, 4H₂ + CO₂ → CH₄ + 2H₂O 반응(ΔG°' = −131 kJ/mol)을 수행한다. 아세트산분해형(acetoclastic) 경로는 CH₃COOH → CH₄ + CO₂(ΔG°' = −36 kJ/mol) 반응으로, Methanosarcina와 Methanotrix(Methanosaeta) 등 제한된 속만이 수행할 수 있다. 메틸영양형(methylotrophic) 경로는 메탄올, 메틸아민, 디메틸설파이드 등 메틸화 화합물을 기질로 사용한다.
세 경로 모두 최종 단계에서 MCR에 의한 메틸-CoM과 CoB의 반응을 통해 메탄이 생성된다. 이 반응(CH₃-S-CoM + HS-CoB → CH₄ + CoM-S-S-CoB, ΔG°' ≈ −30 kJ/mol)은 메탄생성의 공통 종착점이다.
메탄생성균은 다른 생물에서 발견되지 않는 독특한 조효소와 보조인자를 사용한다. 조효소 M(2-메르캅토에탄설폰산)은 자연에서 알려진 가장 작은 유기 조효소로 메틸기를 운반한다. 조효소 B(7-메르캅토헵타노일트레오닌 인산)는 조효소 M과 함께 메탄 형성 반응에 참여한다. 조효소 F₄₂₀는 5-데아자플라빈 유도체로 전자 전달에 관여하며 420 nm에서 특징적인 형광을 발한다. 조효소 F₄₃₀는 니켈을 함유한 테트라피롤(hydrocorphinoid) 화합물로 MCR의 보조인자이며, 그 구조 규명에는 30년 이상의 연구가 소요되었다. 메타노푸란은 CO₂를 최초로 결합하는 보조인자이며, 테트라히드로메타노프테린(H₄MPT)은 C₁ 단위의 환원 과정에서 운반체 역할을 한다.
에너지 보존 메커니즘으로는 화학삼투 결합(Mtr에 의한 Na⁺/H⁺ 펌핑), 전자분기(electron bifurcation), 헤테로디설파이드 환원효소(Hdr)를 통한 에너지 보존 등이 알려져 있다. 메탄생성은 열역학적으로 에너지 수율이 낮은 과정이므로, 이러한 다양한 에너지 보존 전략이 필수적이다.
6. 생태와 환경적 역할
메탄생성균은 지구 탄소 순환의 핵심 구성원으로, 혐기성 환경에서 유기물 분해의 최종 단계를 담당한다. 복잡한 유기물은 여러 단계의 발효를 거쳐 수소, 이산화탄소, 아세트산 등으로 분해되며, 메탄생성균은 이 최종 산물을 메탄으로 전환하여 분해 과정을 완결한다.
전 세계 메탄 배출 총량은 연간 약 580~610 Tg(테라그램)으로 추정되며(Global Methane Budget 2024), 이 중 약 60~70%가 메탄생성균에 의한 생물학적 기원이다. 주요 자연 배출원인 습지는 연간 약 150~220 Tg의 메탄을 배출하여 단일 자연 배출원 중 가장 크다. 반추동물(주로 소)은 연간 약 90~100 Tg, 논토양은 25~50 Tg, 매립지는 50~70 Tg, 흰개미는 10~20 Tg의 메탄을 각각 배출한다.
메탄생성균의 생태적으로 가장 중요한 기능 중 하나는 종간 수소 전달(interspecies hydrogen transfer)이다. 발효 세균이 생성하는 수소를 소비하여 수소 분압을 낮게 유지함으로써, 열역학적으로 불리한 발효 반응이 진행될 수 있게 돕는다. 이러한 공생 관계(syntrophy)가 없으면 혐기성 유기물 분해 전체가 중단될 수 있다.
반추동물의 반추위(rumen)에서 메탄생성균은 셀룰로스 분해 세균, 원생생물과 복잡한 미생물 군집을 형성한다. 한 마리의 소는 하루에 약 70~120 L의 메탄을 주로 트림(eructation, 약 90% 이상)을 통해 배출하며, 이는 섭취 에너지의 약 2~12%에 해당하는 손실이다. 흰개미의 후장에서도 메탄생성균이 셀룰로스 분해 원생생물과 공생하며, 일부는 원생생물 세포 내부에서 세포내 공생을 한다.
해양 퇴적물에서는 메탄생성균의 가까운 친척인 혐기성 메탄영양 고세균(ANME, Anaerobic Methanotrophic Archaea)이 메탄생성을 역방향으로 수행하여 메탄을 산화한다. ANME는 황산염 환원 세균과 공생하여 해양 퇴적물에서 생성되는 메탄의 약 80~90%를 대기 방출 전에 제거하며, 연간 약 200~300 Tg의 메탄을 소비하는 중요한 메탄 싱크(sink) 역할을 한다.
7. 기후 변화와 메탄 저감
메탄은 이산화탄소 다음으로 중요한 인위적 온실가스이다. 100년 기준 GWP는 약 28~34, 20년 기준으로는 약 80~86으로 동일 질량의 이산화탄소보다 훨씬 강력하다. NOAA 자료에 따르면, 대기 중 메탄 농도는 산업화 이전 약 700 ppb에서 2024년 기준 약 1,922~1,930 ppb로 증가하였으며, 이는 지구온난화의 약 30%에 기여하는 것으로 추정된다.
반추동물에서의 메탄 배출 저감을 위한 연구가 활발히 진행되고 있다. 3-니트로옥시프로판올(3-NOP, 상품명 Bovaer)은 MCR의 보조인자 F₄₃₀에 결합하여 메탄 생성을 특이적으로 억제하는 사료 첨가제로, 메타분석 결과 젖소에서 평균 약 30~33%, 조건에 따라 최대 59%까지 메탄 배출을 감소시킬 수 있다. 해조류(Asparagopsis taxiformis 등), 타닌, 사포닌 등 천연 첨가제도 연구되고 있다. 그 외에 메탄생성균에 대한 백신 개발, 낮은 메탄 배출량을 가진 가축의 유전적 선발 등이 시도되고 있다.
기후 변화는 메탄 배출을 증가시키는 양성 피드백 루프를 형성할 가능성이 있다. 북극 영구동토층의 해빙은 동결되어 있던 유기물을 분해 가능하게 하여 메탄 방출을 촉진할 수 있으며, 기온 상승은 습지의 메탄 생성 활동을 증가시킬 수 있다. 해저 메탄 하이드레이트의 불안정화 가능성도 장기적 우려 사항이다.
8. 산업 응용과 바이오가스
메탄생성균은 혐기성 소화(anaerobic digestion)에서 바이오가스를 생산하는 핵심 미생물이다. 하수처리장의 혐기성 소화조에서는 하수 슬러지의 부피를 40~60% 감소시키면서 메탄 약 60~70%, 이산화탄소 약 30~40%로 구성된 바이오가스를 회수한다. 대형 시설에서는 이 바이오가스로 전기 소비의 상당 부분(최대 100%)을 자체 충당할 수 있다.
혐기성 소화조의 최적 운영 조건은 중온성(35~40°C) 또는 고온성(50~60°C), pH 6.8~7.5, 유압 체류 시간(HRT) 15~30일이다. 유기물 과부하는 휘발성 지방산 축적을 초래하여 메탄생성균을 억제하므로 주의가 필요하다.
최근 주목받는 기술로 바이오메타네이션(biomethanation)이 있다. 이는 전기분해로 생성된 수소와 산업 이산화탄소를 메탄생성균을 이용해 메탄으로 전환하는 Power-to-Gas 기술로, 재생 에너지 저장 수단으로서의 잠재력이 크다.
9. 인간 건강과의 관계
인간 장내에서 가장 흔한 메탄생성균은 Methanobrevibacter smithii로, 성인의 약 30~96%에서 검출된다. 이 미생물은 장내 세균이 생성하는 수소를 소비하여 다당류의 효율적인 발효를 돕고, 식이 섬유로부터 더 많은 에너지를 추출하게 한다.
장내 메탄 생성이 과도한 경우 변비, 팽만감 등의 소화기 증상과 연관될 수 있다. 메탄은 장 운동을 늦추는 것으로 알려져 있으며, 메탄 우세형 과민성 대장 증후군(IBS-C) 진단에 호흡 메탄 검사가 활용된다. 공복 시 호흡 메탄 농도가 10 ppm 이상이면 장내 메탄생성균의 활동이 활발한 것으로 간주된다. 일부 연구에서 M. smithii의 풍부도와 비만 사이의 양의 상관관계가 보고되었으나, 결과가 일관되지 않아 인과관계는 아직 불명확하다.
메탄생성균은 현재까지 인간에게 직접적인 병원성이 보고되지 않았다. BSL-1 수준에서 취급되며, 감염성 질환과의 직접적인 관련성은 없는 것으로 간주된다.
10. 극한 환경 적응
메탄생성균은 생물권에서 가장 넓은 온도 범위에 걸쳐 증식할 수 있는 생리 그룹 중 하나이다. 남극 Ace Lake에서 분리된 Methanococcoides burtonii는 −2.5°C에서도 성장하며, 심해 열수분출공의 Methanopyrus kandleri 균주 116은 고압(20 MPa) 환경에서 122°C까지 증식할 수 있다. 이는 현재까지 알려진 모든 생명체 중 가장 높은 성장 온도 기록이다.
M. kandleri의 초고온 적응은 양이온(K⁺, Mg²⁺) 축적, 고유한 보호 분자(사이클릭 2,3-디포스포글리세레이트)에 의한 단백질 안정화, tRNA 수식을 통한 핵산 열안정성 확보 등의 메커니즘에 기인한다. 그러나 흥미롭게도 아미노산 조성 분석에서 M. kandleri는 다른 고온성 메탄생성균과 달리 중온성 종에 가까운 단백질체(proteome) 특성을 보여, 아직 밝혀지지 않은 독특한 열적응 메커니즘의 존재를 시사한다.
일부 호염성(halophilic) 메탄생성균은 5M 이상의 NaCl 농도에서 생존하며, Methanosalsum zhilinae 등 호알칼리성(haloalkaliphilic) 종은 pH 10 이상의 환경에서 서식한다.
11. 연구사와 과학적 의의
메탄생성 현상의 인식은 1776년 Alessandro Volta가 늪지 가스(marsh gas)를 발견한 데서 시작된다. 그러나 메탄이 생물학적 과정의 산물임이 과학적으로 확인된 것은 19세기 후반~20세기 초의 연구들을 통해서였다.
1936년은 메탄생성균 연구의 전환점이다. A. J. Kluyver와 C. B. van Niel은 메탄생성 미생물을 독립적인 분류군으로 인식하고 Methanobacterium과 Methanosarcina 속을 명명하였다. 같은 해 H. A. Barker는 Methanobacterium omelianskii를 최초의 메탄생성균 순수 배양체로 보고하였는데, 이는 나중에 두 종의 공생 혼합 배양임이 밝혀졌다.
1977년 Carl Woese와 George Fox는 16S rRNA 서열 분석을 통해 메탄생성균이 세균(Bacteria)과 근본적으로 다른 새로운 생명 영역에 속한다는 것을 밝히며, 이후 고세균(Archaea)이라는 제3의 생명역을 확립하는 데 결정적 근거를 제공하였다. 이 발견은 생물 분류학의 패러다임을 완전히 바꾼 20세기 생물학의 가장 중요한 업적 중 하나로 평가된다.
이후 1979년 R. S. Wolfe와 W. E. Balch가 혁신적인 혐기 배양 기술을 개발하면서 다양한 메탄생성균의 분리와 특성 규명이 가능해졌다. 2008년 Takai 등은 M. kandleri 균주 116의 122°C 성장을 보고하여 생명 온도 상한 기록을 갱신하였다.
현재 메탄생성균 연구는 기후 변화 대응(메탄 배출 저감), 바이오에너지(바이오가스·Power-to-Gas), 우주생물학(화성 및 외행성 위성에서의 생명 가능성 탐색), 장내 미생물 군집과 건강의 관계 등 다방면에서 활발하게 진행되고 있다. 특히 화성 대기에서 메탄이 검출됨에 따라, 메탄생성균은 외계 생명체 탐사의 모델 생물로서 주목받고 있다.
12. 근연종/유사 미생물 비교
| 특성 | 메탄생성균 | 호염성 고세균(Haloarchaea) | ANME(혐기성 메탄영양 고세균) | 호기성 메탄영양 세균(Methanotrophs) |
|---|---|---|---|---|
| 에너지 대사 | 메탄 생성 | 호흡/발효/광합성 | 메탄 산화(역메탄생성) | 메탄 산화(호기성) |
| 분류 | 고세균(다계통) | 고세균(Halobacteriota) | 고세균(Halobacteriota 등) | 세균(Proteobacteria 등) |
| 산소 요구 | 절대 혐기성 | 호기성/통성 | 절대 혐기성 | 호기성/미호기성 |
| 핵심 효소 | MCR(정방향) | 박테리오로돕신 | MCR(역방향) | 메탄 모노옥시게나아제(MMO) |
| 생태적 역할 | 탄소 무기화, 메탄원 | 고염 환경 분해자 | 해양 메탄 싱크 | 대기 메탄 싱크 |
| 서식 환경 | 혐기성 환경 전반 | 고염 환경(소금 호수 등) | 해양 퇴적물 | 토양, 습지, 담수 |
메탄생성균과 ANME는 MCR 효소를 공유하지만, ANME는 이를 역방향으로 작동시켜 메탄을 산화한다. 이 둘은 계통적으로 가까우며, 메탄생성 경로의 가역성이 진화적으로 활용된 사례로 주목된다.
13. 미해결 질문
메탄생성의 정확한 진화적 기원은 여전히 논쟁 중이다. 메탄생성이 마지막 고세균 공통 조상(LACA)에 존재했는지, 아니면 이후 수평 유전자 전이를 통해 여러 계통에 전파되었는지에 대한 합의가 이루어지지 않았다. DPANN 고세균과 메탄생성균의 진화적 관계, 기후 변화에 따른 영구동토층 해빙이 메탄 배출에 미치는 영향의 규모, 인간 장내 메탄생성균과 비만·대사 장애의 인과관계, 배양 불가능한 환경 메탄생성균의 다양성과 생태적 기능, 반추동물 메탄 배출의 효과적 저감 방법 등이 핵심 연구 과제로 남아 있다.
14. 참고문헌
Kluyver, A.J. & van Niel, C.B. (1936). Prospects for a natural system of classification of bacteria. Zentralbl. Bakteriol. Parasitenkd. Infektionskr. Hyg. Abt. II, 94, 369-403.
Woese, C.R. & Fox, G.E. (1977). Phylogenetic structure of the prokaryotic domain: the primary kingdoms. Proceedings of the National Academy of Sciences, 74(11), 5088-5090. https://doi.org/10.1073/pnas.74.11.5088
Thauer, R.K., Kaster, A.K., Seedorf, H., et al. (2008). Methanogenic archaea: ecologically relevant differences in energy conservation. Nature Reviews Microbiology, 6(8), 579-591. https://doi.org/10.1038/nrmicro1931
Liu, Y. & Whitman, W.B. (2008). Metabolic, phylogenetic, and ecological diversity of the methanogenic archaea. Annals of the New York Academy of Sciences, 1125(1), 171-189. https://doi.org/10.1196/annals.1419.019
Takai, K., Nakamura, K., Toki, T., et al. (2008). Cell proliferation at 122°C and isotopically heavy CH₄ production by a hyperthermophilic methanogen under high-pressure cultivation. PNAS, 105(31), 10949-10954. https://doi.org/10.1073/pnas.0712334105
Saunois, M., Stavert, A.R., Poulter, B., et al. (2020). The global methane budget 2000–2017. Earth System Science Data, 12(3), 1561-1623. https://doi.org/10.5194/essd-12-1561-2020
Lyu, Z., Shao, N., Akinyemi, T., & Whitman, W.B. (2018). Methanogenesis. Current Biology, 28(13), R566-R571. https://doi.org/10.1016/j.cub.2018.05.021
Buan, N.R. (2018). Methanogens: pushing the boundaries of biology. Emerging Topics in Life Sciences, 2(4), 629-646. https://doi.org/10.1042/ETLS20180031
Conrad, R. (2020). Importance of hydrogenotrophic, aceticlastic and methylotrophic methanogenesis for methane production in terrestrial, aquatic and other anoxic environments. Pedosphere, 30(1), 25-39. https://doi.org/10.1016/S1002-0160(19)60823-1
Hook, S.E., Wright, A.D.G., & McBride, B.W. (2010). Methanogens: methane producers of the rumen and mitigation strategies. Archaea, 2010, 945785. https://doi.org/10.1155/2010/945785
Prondzinsky, P., Toyoda, S., & McGlynn, S.E. (2023). The methanogen core and pangenome: conservation and variability across biology's growth temperature extremes. Microbial Genomics, 9(1), dsac048. https://doi.org/10.1093/femsml/uqac008
Adam, P.S., Borrel, G., & Gribaldo, S. (2023). The origin and evolution of methanogenesis and Archaea are intertwined. PNAS Nexus, 2(2), pgad023. https://doi.org/10.1093/pnasnexus/pgad023
Garcia, J.L., Patel, B.K.C., & Ollivier, B. (2000). Taxonomic, phylogenetic, and ecological diversity of methanogenic Archaea. Anaerobe, 6(4), 205-226. https://doi.org/10.1006/anae.2000.0345
Enzmann, F., Mayer, F., Rother, M., & Holtmann, D. (2018). Methanogens: biochemical background and biotechnological applications. AMB Express, 8(1), 1-22. https://doi.org/10.1186/s13568-017-0531-x
Dridi, B., Henry, M., El Khéchine, A., Raoult, D., & Drancourt, M. (2009). High prevalence of Methanobrevibacter smithii and Methanosphaera stadtmanae detected in the human gut using an improved DNA detection protocol. PLoS ONE, 4(9), e7063. https://doi.org/10.1371/journal.pone.0007063
Hanišáková, N., Vítězová, M., et al. (2022). The historical development of cultivation techniques for methanogens and other strict anaerobes and their application in modern microbiology. Microorganisms, 10(2), 412. https://doi.org/10.3390/microorganisms10020412
Saunois, M., Stavert, A.R., Poulter, B., et al. (2024). Global Methane Budget 2000-2020. Earth System Science Data, 17, 1873-1958. https://doi.org/10.5194/essd-17-1873-2025
재미있는 사실
메탄생성균은 지구에서 가장 오래된 생물군 중 하나로, 약 35억 년 전부터 존재했을 것으로 추정됩니다. 초기 지구의 산소 없는 대기는 메탄생성에 이상적이었으며, 약 24억 년 전 산소 대폭발 사건 이후에도 이들은 혐기성 환경으로 물러나 오늘날까지 생존하고 있습니다.
Methanopyrus kandleri 균주 116은 122°C에서도 증식할 수 있어, 현재까지 알려진 모든 생명체 중 가장 높은 성장 온도 기록을 보유하고 있습니다. 이 온도는 물의 끓는점보다 높으며, 일반 가정용 압력솥 내부 온도(약 120°C)와 비슷합니다.
전 세계 소는 연간 약 1억 톤(100 Tg)의 메탄을 배출하며, 이는 전체 인위적 메탄 배출의 약 15~17%에 해당합니다. 한 마리의 소는 하루에 약 70~120 리터의 메탄을 트림으로 배출하는데, 이는 차량이 약 30~50 km를 주행할 때 배출하는 탄소량과 비슷합니다.
메탄생성균은 조효소 F₄₂₀ 덕분에 자외선(420 nm)을 받으면 청록색으로 빛나는 독특한 형광 특성을 가집니다. 이 '빛나는' 특성 덕분에 과학자들은 복잡한 미생물 군집에서 메탄생성균을 형광현미경으로 간편하게 식별할 수 있습니다.
메탄생성균의 발견은 생물학 역사를 바꿨습니다. 1977년 Carl Woese가 메탄생성균의 16S rRNA를 분석하여 이들이 세균과 완전히 다른 생명체임을 밝힘으로써, 생물을 세 영역(세균·고세균·진핵생물)으로 나누는 현대 분류 체계가 탄생했습니다.
해양 퇴적물에서 생성되는 메탄의 약 80~90%는 대기로 방출되기 전에 ANME(혐기성 메탄영양 고세균)에 의해 제거됩니다. 이 '메탄 필터'가 없다면 해양에서 연간 200~300 Tg의 메탄이 추가로 대기에 유입되어 지구온난화가 크게 가속화될 것입니다.
메탄생성균이 사용하는 조효소 M(2-메르캅토에탄설폰산)은 자연에서 알려진 가장 작은 유기 조효소입니다. 또한 조효소 F₄₃₀는 니켈을 함유한 극히 독특한 분자로, 자연에서 메탄생성균에서만 발견되며 그 구조 규명에 30년 이상이 소요되었습니다.
인간 장내에서 가장 흔한 메탄생성균인 Methanobrevibacter smithii는 성인의 약 30~96%에서 발견됩니다. 이 미생물은 장내 세균이 생성하는 수소를 제거하여 식이 섬유의 효율적인 소화를 돕지만, 그 결과 더 많은 칼로리를 흡수하게 되어 비만과의 연관성이 연구되고 있습니다.
흰개미 후장에는 메탄생성균이 공생하며, 전 세계 흰개미는 연간 약 10~20 Tg의 메탄을 배출합니다. 작은 곤충이지만 기후에 무시할 수 없는 영향을 미치는 셈입니다. 일부 메탄생성균은 흰개미 장내 원생생물의 세포 안에서 공생하는 것으로 알려져 있습니다.
대형 하수처리장은 메탄생성균이 생산하는 바이오가스로 시설 전기 소비의 상당 부분, 경우에 따라서는 100%를 자체 충당할 수 있습니다. 유기 폐기물을 처리하면서 동시에 재생 에너지를 생산하는 일석이조의 기술입니다.
메탄생성균은 지구에서 가장 넓은 온도 범위에 걸쳐 증식하는 생리 그룹 중 하나입니다. 남극 호수의 −2.5°C부터 심해 열수분출공의 122°C까지, 무려 124.5°C의 온도 범위에서 성장할 수 있는 종들이 존재합니다.
FAQ
메탄생성균은 모두 고세균(Archaea)에 속합니다. 세균(Bacteria)과 고세균은 둘 다 원핵생물이지만, 세포벽 구조, 세포막 지질 조성(에테르 결합 vs. 에스테르 결합), 유전체 특성 등에서 근본적인 차이가 있습니다. 실제로 1977년 Carl Woese가 메탄생성균의 16S rRNA 서열을 분석하여 고세균이라는 새로운 생명 영역을 제안하는 결정적 근거를 제공했습니다. 메탄 생성 대사는 고세균에서만 발견되는 독특한 특성입니다.
메탄생성균은 절대 혐기성 미생물로, 산소에 노출되면 수분 내에 사멸합니다. 이는 메탄생성에 필수적인 효소들, 특히 MCR(메틸-조효소 M 환원효소)과 그 보조인자 F₄₃₀(니켈 함유 테트라피롤)가 산소에 의해 비가역적으로 산화·손상되기 때문입니다. 또한 대부분의 메탄생성균은 활성산소종(ROS)을 해독하는 효소(카탈라아제, 슈퍼옥사이드 디스뮤타아제)가 부족하거나 결여되어 있어 산소 독성에 대한 방어 능력이 극히 제한적입니다.
흔히 알려진 것과 달리, 반추동물의 메탄은 대부분(약 90% 이상) 트림(eructation)을 통해 배출됩니다. 메탄은 반추위(rumen)에서 생성되며, 되새김질 과정에서 가스가 함께 입을 통해 배출됩니다. 장에서 생성되어 방귀로 배출되는 양은 전체의 약 10% 미만입니다.
이론적으로 가능하며, 일부 분야에서는 실질적 성과가 나오고 있습니다. 대표적으로 3-NOP(상품명 Bovaer)라는 사료 첨가제가 젖소에서 평균 약 30~33%의 메탄 배출 감소 효과를 보이며, 일부 연구에서는 최대 59%까지 감소가 보고되었습니다. 그러나 습지 등 자연 환경에서의 메탄 배출을 인위적으로 억제하는 것은 생태계에 예측 불가능한 영향을 미칠 수 있어 권장되지 않습니다. 기후 변화 대응은 축산 부문의 메탄 저감, 매립지 가스 포집, 논물 관리 개선 등 제어 가능한 영역에 집중되고 있습니다.
메탄생성 현상 자체는 1776년 Alessandro Volta가 습지 가스(marsh gas)를 발견하면서 알려졌습니다. 1936년 네덜란드의 A. J. Kluyver와 C. B. van Niel이 메탄생성 미생물을 독립적인 분류군으로 인식하고 Methanobacterium과 Methanosarcina 속을 명명하였습니다. 같은 해 H. A. Barker는 Methanobacterium omelianskii의 배양을 보고했습니다(후일 혼합 배양으로 판명). 결정적 전환점은 1977년 Carl Woese가 16S rRNA 분석을 통해 메탄생성균이 세균과 구별되는 새로운 생명 영역(고세균)에 속한다는 것을 밝힌 것입니다.
메탄생성균은 극한 환경(고온·고압·고염·알칼리)에서 생존하고, 간단한 무기 화합물(H₂, CO₂)만으로 에너지를 얻으며, 산소 없이 성장할 수 있습니다. 이러한 특성은 초기 지구와 유사한 조건뿐 아니라 화성이나 외행성 위성의 환경과도 일치합니다. 실제로 화성 대기에서 계절적 메탄 변동이 관측되어 생물학적 기원 가능성이 제기되고 있으며, 목성의 위성 유로파나 토성의 위성 엔셀라두스의 지하 해양에서 메탄생성균과 유사한 생명체가 존재할 수 있다는 가설이 활발히 연구되고 있습니다.
Methanopyrus kandleri 균주 116은 고압(20 MPa) 하에서 122°C까지 증식 가능하며, 이는 현존 생명체의 성장 온도 상한 기록입니다. 고압은 물의 끓는점을 높여 세포가 액체 환경에서 기능할 수 있게 합니다. 단백질 안정화에는 양이온(K⁺, Mg²⁺)과 특수 보호 분자(사이클릭 2,3-디포스포글리세레이트)가 기여하며, tRNA 수식을 통해 핵산 열안정성도 확보합니다. 흥미롭게도 이 종의 단백질체 아미노산 조성은 다른 고온성 종과 달리 중온성 종에 가까워, 아직 밝혀지지 않은 독특한 열적응 메커니즘이 있을 것으로 추정됩니다.
네, 메탄생성균은 조효소 F₄₂₀ 덕분에 독특한 자가형광 특성을 가집니다. 420 nm 파장의 자외선을 조사하면 청록색(약 470 nm) 형광을 발하므로, 형광현미경으로 관찰하면 다른 미생물과 구별하여 식별할 수 있습니다. 이 방법은 복잡한 미생물 군집(혐기성 소화 슬러지, 반추위 내용물 등)에서 메탄생성균을 정량하는 데 실용적으로 활용됩니다. 분자생물학적으로는 mcrA 유전자를 표적으로 한 PCR이 메탄생성균 검출의 표준 방법입니다.
메탄생성균은 혐기성 환경에서 유기물 분해 사슬의 최종 단계를 담당합니다. 이들이 없으면 발효 과정에서 생성되는 수소가 축적되어 수소 분압이 높아지고, 이에 따라 상류의 발효 반응 자체가 열역학적으로 중단됩니다. 결과적으로 습지, 퇴적물, 동물 소화관 등에서의 유기물 분해가 정체되어 물질 순환이 크게 교란될 것입니다. 또한 반추동물은 효율적인 셀룰로스 소화가 불가능해져 생존에 심각한 영향을 받을 것입니다.
갤러리
4 장의 이미지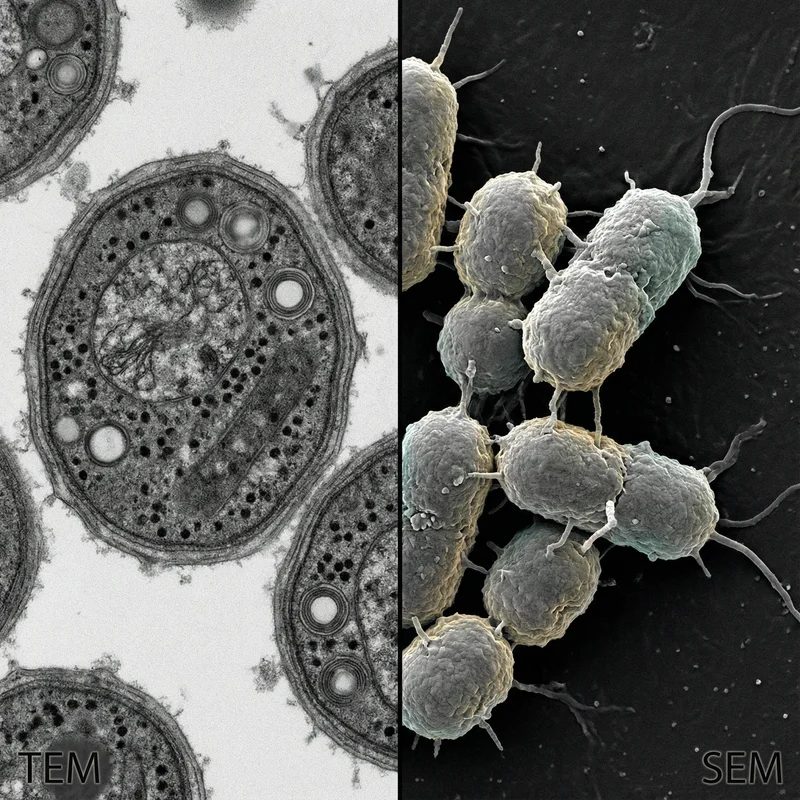 메탄생성균
메탄생성균메탄생성균
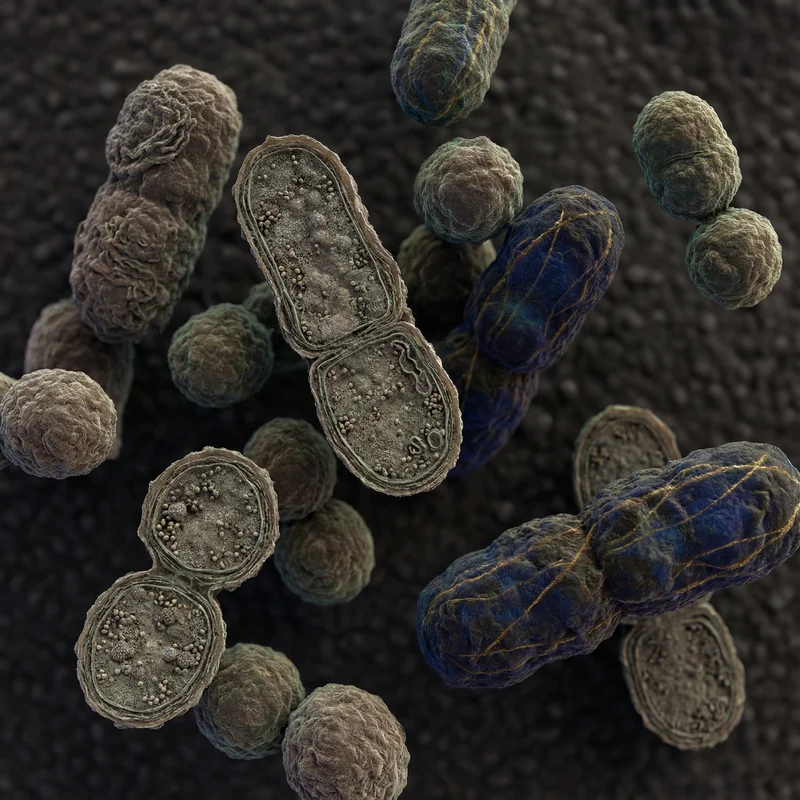 메탄생성균
메탄생성균메탄생성균
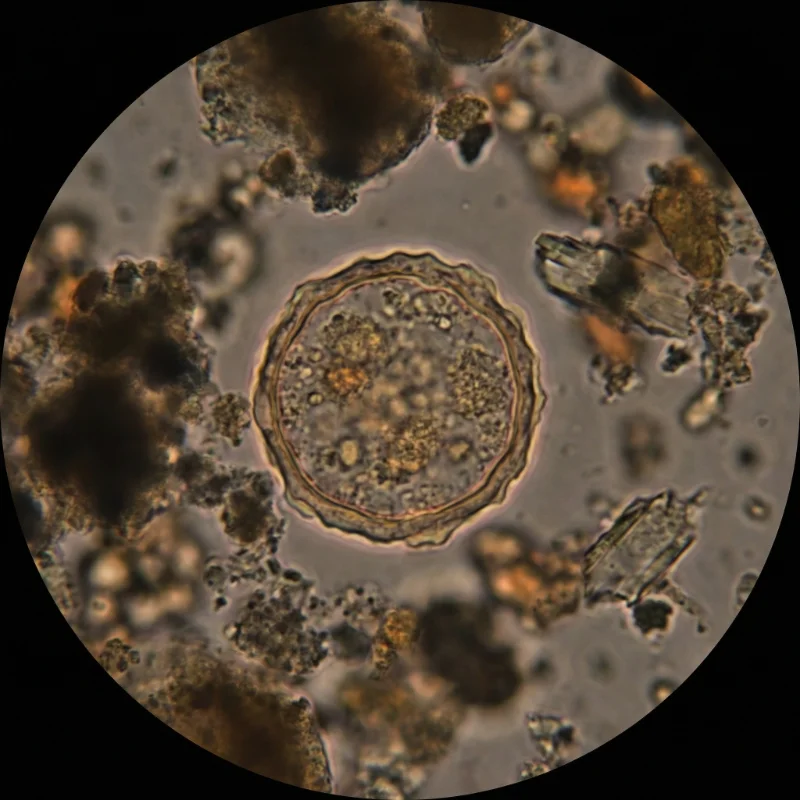 메탄생성균
메탄생성균메탄생성균
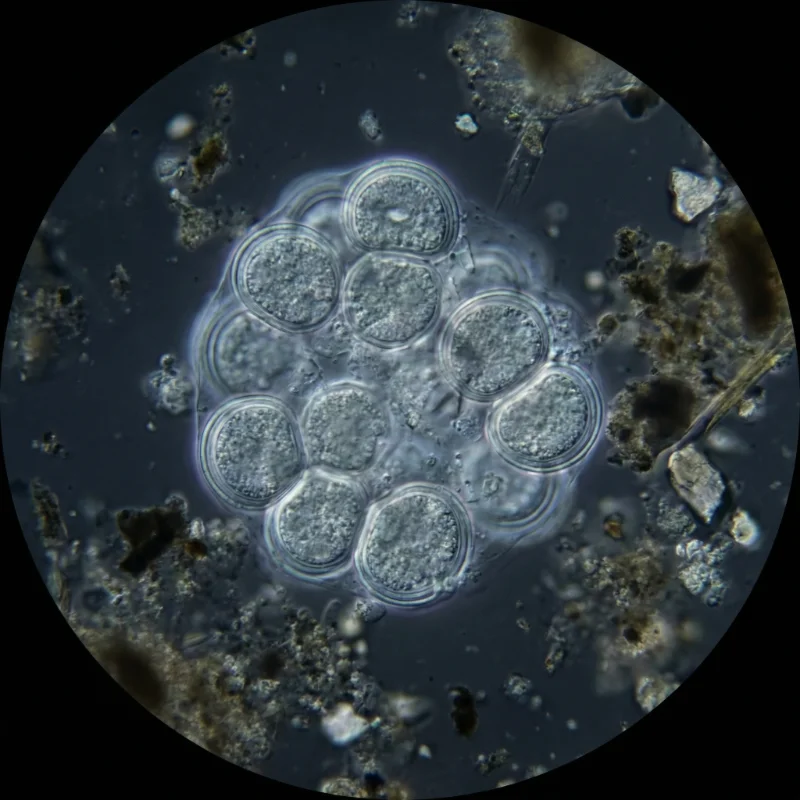 메탄생성균
메탄생성균메탄생성균